В настоящее время композиты составляют одну из наиболее важных групп материалов в стоматологической практике. Они используются при пломбировании всех групп зубов, герметизации фиссур, для фиксации ортопедических конструкций, в качестве облицовочных композитов [3]. Наибольшее распространение получили материалы, органическая матрица которых представляет собой сополимер акриловых и эпоксидных смол, одним из основных мономеров которого является бисфенол – глицидилметакрилат (Bis-GMA) [5], комономерами выступают триэтиленгликольдиметакрилат (TEGDMA) и уретандиметилметакрилат (UDMA). Соотношение и состав мономеров варьируются в зависимости от специфики использования, а также от производителя полимера [2, 9, 10]. Принципиально новыми по химическому строению являются композиты Tet-Sil на основе оксиранов и силоранов – мономеров с открытыми кольцами, не содержащих метакриловые группы. Данные пломбировочные материалы разработаны для уменьшения и преодоления полимеризационной усадки. Очевидно, что различия типов мономеров в составе композита определяют свойства материала, оказывают влияние на степень его полимеризации, биодеградации, химической реактивности [11].
Для оценки потенциального риска возникновения неблагоприятных реакций, обусловленных стоматологическими материалами, изучают преимущественно физические, химические и механические свойства полимера [8, 12]. С целью определения биосовместимости на доклиническом этапе в настоящее время используют изучение цитотоксичности на культуре клеток мышиных фибробластов, контактные тесты полимеров с базофилами цельной крови человека для выявления выброса гистамина, имплантацию композита в ткани полости рта лабораторных животных [1, 4, 6, 7, 9, 13, 14]. Данные методы являются трудоемкими, дорогостоящими, требуют наличия специального оборудования и не дают возможности определить индивидуальную реакцию организма на пломбировочный материал в конкретной клинической ситуации. В этом плане актуально создание новых in vitro тестов для изучения биосовместимости полимерных стоматологических материалов, оптимизации клинического выбора композита.
Цель исследования: изучить характер влияния композитов на структурно-функциональные свойства клеток крови в модельных опытах для определения биосовместимости стоматологических материалов.
Материалы и методы исследования
В исследовании принимали участие 60 соматических здоровых лиц с санированной полостью рта в возрасте от 18 до 21 года. Материалом служила венозная кровь, взятая стандартным методом. Контрольную группу составили 22 человека, экспериментальную – 38 человек. Влияние метакрилата и оксирана изучали в двух подгруппах, действуя на образцы крови неполимеризованным и полимеризованным материалом.
Исследование структурно-функциональных характеристик клеток крови осуществлялось с использованием автоматического гематологического анализатора Sismex КХ-21 до и после 30-минутной инкубации с композитами. Также после предварительного окрашивания по методу Лейшмана проводилась ультрамикроскопия препаратов крови на микроскопе Zeiss Axiostar (×1500). Статистическую обработку полученных результатов проводили с помощью компьютерной программы «ANOVA».
Таблица 1
Влияние неполимеризованного и полимеризованного материала на основе метакрилата на гематологические показатели (M ± St.dev.)
|
№ п/п |
Показатели |
Контрольная группа (n = 22) |
Экспериментальная группа, неполимеризованный материал (n = 19) |
Экспериментальная группа, полимеризованный материал (n = 19) |
|
1 |
Лейкоциты (WBC, × 109/л) |
6,10 ± 0,45 |
5,97 ± 0,40 |
6,18 ± 0,56 |
|
2 |
Эритроциты (RBC, × 1012/л) |
4,90 ± 0,15 |
5,06 ± 0,15 |
5,27 ± 0,14* |
|
3 |
Гемоглобин (HGB, × 10 г/л) |
14,33 ± 0,44 |
15,34 ± 0,54* |
15,74 ± 0,41* |
|
4 |
Гематокрит (HCT, %) |
43,11 ± 1,29 |
45,79 ± 1,44* |
46,29 ± 1,28* |
|
5 |
Средний объем эритроцитов (MCV, фл) |
88,01 ± 0,57 |
88,40 ± 0,58 |
87,86 ± 0,70 |
|
6 |
Среднее объемного содержания гемоглобина в эритроците (MCH; пг) |
29,21 ± 0,18 |
30,25 ± 0,32 |
29,88 ± 0,27 |
|
7 |
Среднее содержание гемоглобина (MCHC; г/л) |
33,26 ± 0,18 |
34,22 ± 0,28 |
34,03 ± 0,27 |
|
8 |
Тромбоциты (PLT, ×109/л) |
248,06 ± 20,03 |
247,08 ± 22,22 |
237,94 ± 19,61* |
|
9 |
Лимфоциты (LYM, %) |
34,56 ± 2,04 |
33,36 ± 1,93 |
33,03 ± 2,29 |
|
10 |
Клетки среднего размера(MXD, %) |
10,79 ± 1,13 |
11,21 ± 2,35 |
8,78 ± 1,82* |
|
11 |
Нейтрофилы (NEUT, %) |
55,48 ± 3,89 |
56,24 ± 4,68 |
60,88 ± 4,33* |
|
12 |
Абсолютное число лейкоцитов в/мкл цельной крови (LYM) |
2,09 ± 0,16 |
1,96 ± 0,15 |
2,00 ± 0,19 |
|
13 |
Абсолютное число базофилов, эозинофилов и моноцитов в/мкл цельной крови (MXD) |
0,74 ± 0,09 |
0,70 ± 0,13 |
0,67 ± 0,15 |
|
14 |
Абсолютное число нейтрофилов в/мкл цельной крови(NEUT) |
3,92 ± 0,45 |
3,82 ± 0,47 |
4,20 ± 0,69 |
|
15 |
Взвешенное распределение тромбоцитов (PDW, фл) |
13,79 ± 0,42 |
13,82 ± 0,49 |
14,57 ± 0,56 |
|
16 |
Средний объем тромбоцита (MPV, фл) |
10,89 ± 0,23 |
10,86 ± 0,22 |
11,28 ± 0,24 |
Примечание. *p = 0,01.
Результаты исследования и их обсуждение
При анализе полученных результатов выявлено, что после инкубации цельной крови с неполимеризованным материалом на основе метакрилата имеется тенденция к увеличению содержания гемоглобина, гематокрита, что, вероятно, обусловлено склеиванием и агрегацией эритроцитов, изменением формы клеток, что отражается на детекции (табл. 1).
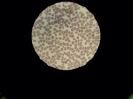
Полученные данные подтверждаются при проведении ультрамикроскопии изучаемых образцов. Так, при микроскопии препаратов крови контрольной группы обнаружены эритроциты обычной формы с центральным просветлением (рис. 1, А). В препаратах крови после инкубации с неполимеризованным материалом на основе метакрилата заметно склеивание, агрегация эритроцитов (++++), выраженная деформация мембраны, которая приобретает бугристую форму (рис. 1, Б).
Под влиянием полимеризованного метакрилата происходит более выраженное увеличение концентрации гемоглобина (+ 10,0 %, р = 0,01), значения гематокрита (+ 7,4 %, р = 0,01), которое, вероятно, обусловлено агрегацией эритроцитов, что отчетливо наблюдается при микроскопии данных образцов (рис. 1, В). Кроме того, выявлены явления склеивания, агрегации эритроцитов, так называемые «монетные столбики», определяется сгущение и увеличение количества эритроцитов в поле зрения, обнаруживается явление пойкилоцитоза (овалоцитоза).
Также выявлено влияние исследуемого материала на показатели лейкоцитарного ряда. Отмечается выраженное снижение количества клеток MXD-группы – моноцитов, эозинофилов, базофилов на 18,6 % относительно значения в контроле (р = 0,01), увеличение количества нейтрофилов на 9,7 % (р = 0,01), отражающее сдвиги в лейкоцитарной формуле. Обнаружена тенденция к снижению количества тромбоцитов (табл. 1).
При оценке показателей клеточного состава крови, инкубированной с материалом на основе оксирана, выявлено увеличение содержания гемоглобина (+ 13,0 %; р ≤ 0,01), тенденция к увеличению гематокрита (+ 9,0 %, р = 0,01) (табл. 2).
При микроскопии в образцах крови после инкубации с неполимеризованным материалом на основе оксирана определяется изменение формы и усиление агрегации эритроцитов с большим количеством агрегатов (++++) (рис. 2, Б).
При сравнении гематологических показателей после инкубации с полимеризованными порциями материала с показателями контрольной группы определяется тенденция к увеличению гематокрита (+ 8,2 %; р = 0,01), количества эритроцитов, содержания гемоглобина (+ 8,1 % и + 12,3 % соответственно; р = 0,01) (табл. 2).
Выявляются также изменения в лейкоцитарной формуле, проявляющиеся в снижении количества MXD-клеток на 15,3 % (р = 0,01), увеличении количества нейтрофилов на 10,6 % (р = 0,01), тенденции к снижению числа лимфоцитов. Данные изменения, вероятно, обусловлены фиксацией клеток в белковом монослое, образующемся на поверхности полимера при его взаимодействии с кровью.
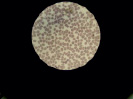
Примечательным является тот факт, что при микроскопии образцов крови после инкубации с полимеризованным материалом на основе оксирана картина приближена к норме. Определяется монослой эритроцитов без выраженной агрегации (рис. 2, В).
 А)
А) 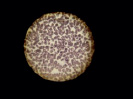 Б)
Б)  В)
В)
Рис. 1. Препараты крови, инкубированной с композитом на основе метакрилата: А – контрольный образец, Б – препарат крови, инкубированной с неполимеризованным материалом, В – препарат крови, инкубированной с полимеризованным материалом
Таблица 2
Влияние неполимеризованного и полимеризованного материала на основе оксирана на показатели клеточного состава крови (M ± St.dev.)
|
№ п/п |
Показатели |
Контрольная группа (n = 22) |
Экспериментальная группа, неполимеризованный материал (n = 19) |
Экспериментальная группа, полимеризованный материал (n = 19) |
|
1 |
Лейкоциты (WBC, × 109/л) |
6,10 ± 0,45 |
5,96 ± 0,46 |
6,12 ± 0,53 |
|
2 |
Эритроциты (RBC, × 1012/л) |
4,90 ± 0,15 |
5,31 ± 0,14 |
5,30 ± 0,14* |
|
3 |
Гемоглобин (HGB, × 10 г/л) |
14,33 ± 0,44 |
16,20 ± 0,52* |
16,09 ± 0,52* |
|
4 |
Гематокрит (HCT, %) |
43,11 ± 1,29 |
46,98 ± 1,30* |
46,65 ± 1,29* |
|
5 |
Средний объем эритроцитов (MCV, фл) |
88,01 ± 0,57 |
88,54 ± 0,58 |
87,98 ± 0,69 |
|
6 |
Среднее объемного содержания гемоглобина в эритроците (MCH; пг) |
29,21 ± 0,18 |
30,49 ± 0,34 |
30,33 ± 0,36 |
|
7 |
Среднее содержание гемоглобина (MCHC; г/л) |
33,26 ± 0,18 |
34,44 ± 0,28 |
34,46 ± 0,30 |
|
8 |
Тромбоциты (PLT, ×109/л) |
248,06 ± 20,03 |
243,42 ± 23,65 |
226,35 ± 19,71* |
|
9 |
Лимфоциты (LYM, %) |
35,15 ± 2,04 |
33,90 ± 1,61 |
33,31 ± 2,21* |
|
10 |
Клетки среднего размера (MXD, %) |
12,12 ± 1,41 |
12,74 ± 1,75 |
10,27 ± 2,65* |
|
11 |
Нейтрофилы (NEUT, %) |
50,75 ± 4,79 |
52,30 ± 4,28 |
56,15 ± 4,57* |
|
12 |
Абсолютное число лейкоцитов в/мкл цельной крови (LYM) |
2,09 ± 0,16 |
1,99 ± 0,15 |
2,03 ± 0,18 |
|
13 |
Абсолютное число базофилов, эозинофилов и моноцитов в/мкл цельной крови (MXD) |
0,71 ± 0,12 |
0,79 ± 0,11 |
0,75 ± 0,20 |
|
14 |
Абсолютное число нейтрофилов в/мкл цельной крови (NEUT) |
3,90 ± 0,57 |
3,73 ± 0,59 |
3,63 ± 0,55 |
|
15 |
Взвешенное распределение тромбоцитов (PDW, фл) |
13,79 ± 0,42 |
13,85 ± 0,46 |
14,48 ± 0,53 |
|
16 |
Средний объем тромбоцита (MPV, фл) |
10,89 ± 0,23 |
11,07 ± 0,23 |
11,26 ± 0,25 |
|
17 |
Отношение ( %) объема крупных тромбоцитов ко всему объему тромбоцитов (P-LCR) |
32,29 ± 1,90 |
33,44 ± 1,88 |
35,24 ± 2,03 |
Примечание. *p = 0,01.
 А)
А) 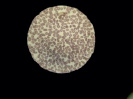 Б)
Б) 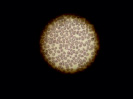 В)
В)
Рис. 2. Препараты крови, инкубированной с композитом на основе оксирана: А – контрольный образец, Б – препарат крови, инкубированной с неполимеризованным материалом, В – препарат крови, инкубированной с полимеризованным материалом
Заключение
Таким образом, полученные результаты позволяют использовать разработанную экспериментальную модель для определения биосовместимости полимерных стоматологических материалов, осуществлять индивидуальный подбор композита в каждом конкретном клиническом случае. Применение данных in vitro тестов выявило мембраноповреждающее действие метакрилата и оксирана, отражающееся в изменениях структурно-функциональных характеристик клеток крови. Причем метакрилат обладает более выраженным повреждающим потенциалом по сравнению с оксираном. Негативное действие композита вследствие биодеградации после полимеризации требует тщательного соблюдения режимов окончательной обработки пломб. Полимеризованные композиты на основе оксирана биоинертны, что дает возможность рекомендовать их для более широкого применения.
Рецензенты:
Тлустенко В.П., д.м.н., профессор, заведующая кафедрой ортопедической стоматологии ГБОУ ВПО СамГМУ Минздрава России, г. Самара;
Кретова И.Г., д.м.н., профессор, заведующая кафедрой безопасности жизнедеятельности и физического воспитания ФГБОУ ВПО «Самарский государственный университет», г. Самара.
Библиографическая ссылка
Гильмияров Э.М., Радомская В.М., Гильмиярова Ф.Н., Мякишева Ю.В., Быков И.М., Доменюк Д.А., Гильмиярова И.Е., Свечникова М.В., Волков Е.Д., Филиппова М.Д. ВЛИЯНИЕ МОНОМЕРОВ КОМПОЗИТНЫХ СТОМАТОЛОГИЧЕСКИХ МАТЕРИАЛОВ НА СТРУКТУРНО-ФУНКЦИОНАЛЬНЫЕ ХАРАКТЕРИСТИКИ КЛЕТОК КРОВИ // Фундаментальные исследования. 2015. № 1-5. С. 920-924;URL: https://fundamental-research.ru/ru/article/view?id=37487 (дата обращения: 15.05.2026).



