Цветки пижмы обыкновенной (Flores Tanaceti) семейства Астровые (Asteracea) используются в медицине как желчегонное и противоглистное средство в виде настоя, отвара и сухого экстракта – препарат «Танацехол», основными действующими веществами которого являются флавоноиды. Цветки пижмы обыкновенной имеют сложный химический состав, представленный помимо флавоноидов эфирными маслами, гидроксикоричными кислотами, дубильными веществами, полисахаридами [4] .
Пектиновые полисахариды, выделенные из разных растительных источников, характеризуются разнообразием боковых структур, нерегулярностью, блочным строением молекул, что и определяет широкий спектр их фармакологического действия [7]. В настоящее время основной задачей изучения пектинов является выяснение взаимосвязи их химического строения с биологическим действием и фармакологической активностью с целью обоснования их более широкого применения в качестве лекарственных средств.
Материалы и методы исследования
Полисахаридный комплекс цветков пижмы обыкновенной (ПСП) выделяли из воздушно-сухих цветков пижмы обыкновенной («Цветки пижмы», ООО «Здоровье», Россия). Полифенольные соединения отделяли предварительной экстракцией 40 %-м этанолом. Из полученного шрота трехкратной экстракцией 1 %-м раствором оксалата аммония в течение 1,5 часов извлекали ПСП, который осаждали избытком этанола. Очистку проводили этанолом, ацетоном и эфиром. В предварительных исследованиях был изучен состав, физико-химические свойства и предложен метод стандартизации ПСП [2].
Для изучения противовоспалительной, антиоксидантной и гастропротекторной активности использовали 3 %-й раствор ПСП в дозе 0,3 г/кг массы [5]. Исследование проводили на 84 аутбредных крысах линии CD (Sprague Dawley), массой 150–200 г, полученных из питомника «Столбовая», содержащихся в стандартных условиях вивария. Исследования на животных выполнены в соответствии с «Правилами проведения работ с использованием экспериментальных животных» (приказ МЗ РФ 708н от 23.08.2010).
Для изучения противовоспалительной и антиоксидантной активности 56 животных были разделены на 4 группы по 14 особей. Воспалительную реакцию моделировали введением 0,1 мл 2,5 %-го раствора формалина под апоневроз правой задней конечности крысы (серия контроль патологии). Первой группе подопытных крыс за 2 часа до введения флогогенного агента, затем с интервалом 2 часа, в последующие 7 суток однократно внутрижелудочно (через зонд) вводили ПСП. Вторая группа животных получала препарат сравнения – диклофенак натрия (Диклофенак, ООО «Хемофарм», Россия) в дозе 11 мг/кг массы в режиме назначения полисахарида [1]. Третьей группе в те же сроки вводили комбинацию ПСП в дозе 0,3 г/кг массы и диклофенака натрия в дозе 11 мг/кг массы. Животные контрольной группы получали физиологический раствор в эквиобъеме в режиме назначения ПСП.
Величину отека конечности крыс измеряли онкометрически на цифровом плетизмометре StoeltingCo (США) через 1, 2, 3, 4, 6 и 24 часа после введения формалина, далее один раз в сутки в течение 7 дней. Динамику воспалительной реакции контролировали также по уровню лейкоцитов и величине СОЭ через 4 часа, на 3 и 7 сутки после начала эксперимента во всех группах (n = 7). Состояние ПОЛ и антиоксидантной защиты по всех сериях (n = 7) оценивали по уровню малонового диальдегида (МДА), тиоловых групп (GSH), глутатион-S-трансферазы (GST) и глутатионпероксидазы (GPх) в лизате эритроцитов. Кровь для исследований у подопытных животных забирали через 4 часа и 7 суток после моделирования воспалительной реакции из брюшной аорты под эфирным наркозом. Исследуемые показатели определяли следующим образом: концентрацию малонового диальдегида (МДА) по реакции с тиобарбитуровой кислотой (по методу Стальной Д.И., Горишвили Т.Г., 1977), уровень безбелковых тиоловых групп (GSH) по реакции восстановления дисульфид-5,5-дитиобис-2-нитробензоата (по методу Habeeb, 1972) на спектрофотометре ShimadzuUV-150-02, активность глутатионпероксидазы (GPх) по реакции ферментативного восстановления глутатиона гидроперекисью третбутила (по методу Paglia D.E., Valentine W.N., 1967 в модификации Ланкина В.З.), активность глутатион-S-трансферазы (GST) по методу J.N. Keen, W.B. Iakoby (1978) с использованием биохимического анализатора Humalyzer 2000.
Исследование гастропротекторной активности ПСП проводили на 28 животных, разделенных на 4 группы (n = 7). Язвы моделировали внутрижелудочным (через зонд) введением индометацина (Индометацин, «Софарма», Болгария) в дозе 20 мг/кг дважды с интервалом в 4 ч (контроль патологии) [3]. Первой группе животных вводили ПСП ежедневно внутрижелудочно в течение 3 суток, на 4 сутки дважды – за час до 1-го и 2-го введения индометацина. Эффективность препарата оценивали через 16 часов после воздействия ульцерогенного агента по результатам макроскопического исследования желудка на наличие язв. Деструкции дифференцировали на точечные (менее 1 мм), полосовидные и крупные (более 1 мм). Подсчитывали среднее количество изъязвлений на каждое животное в группе; процент животных с язвами; рассчитывали индекс Паулса (суммарный показатель количества деструкций) и противоязвенную активность препарата (отношение индекса Паулса в контрольной группе к индексу Паулса в опытной группе) [3]. Вторая и третья группы животных получали препараты сравнения – омепразол (Омепразол, ООО «ПроМед», Россия) в дозе 20 мг/кг массы [9] и ранитидин в дозе 25 мг/кг массы (Ранитидин, ООО «Озон», Россия) [6] в режиме назначения полисахарида.
Статистическую обработку полученных результатов проводили с использованием прикладных программ MSExel 2010 и Statsoft Statistica 8.0. Характер распределения данных оценивали по критерию Шапиро – Уилкса, наличие статистически достоверных межгрупповых различий определяли по t–критерию Стьюдента.
Результаты исследования и их обсуждение
Выделенный полисахаридный комплекс цветков пижмы обыкновенной представляет собой аморфное вещество светло-серого цвета. Был установлен моносахаридный состав ПСП (методом тонкослойной хроматографии): глюкоза, галактоза, ксилоза и арабиноза. Высокое содержание уроновых кислот (84,70 %) позволяет отнести выделенный комплекс к классу гликуроногликанов типа пектиновых веществ [2].
Введение формалина животным контрольной группы приводило к гиперемии и нарастанию отека конечности с максимумом через 4 часа. В последующие сроки наблюдения отек постепенно уменьшался и объем конечности достигал нормы на 7-е сутки опыта. Воспалительная реакция сопровождалась лейкоцитозом, количество лейкоцитов через 4 часа после введения флогогенного агента возросло в 3 раза по сравнению с уровнем у интактных животных (р < 0,05). Максимальный подъем СОЭ на 133,3 % по сравнению с данными интактных животных (р < 0,05) наблюдали на 3-е сутки исследования.
У животных, получавших ПСП, через 4 часа после введения формалина отек воспаленной конечности уменьшился на 8,97 % (р < 0,05) по сравнению с серией контроля патологии. Восстановление объема конечности отмечалось на пятые сутки опыта. Через 4 часа после введения ПСП снижался уровень лейкоцитов на 38,67 % (р < 0,05) и СОЭ (р > 0,05) по сравнению с контролем. Нормализация показателей СОЭ и количества лейкоцитов наблюдалась на 7 сутки эксперимента. Полученные данные представлены в табл. 1.
У животных, получавших диклофенак натрия, через 4 часа после введения формалина интенсивность отека снизилась на 7,24 % (р < 0,05), уровень лейкоцитов на 52,79 % (р < 0,05), величина СОЭ не менялась по сравнению с контролем патологии. Возвращение всех показателей к норме наблюдалось на пятые сутки эксперимента.
Лечение экссудативного воспаления комбинацией ПСП и диклофенака натрия существенно не меняло динамику отека конечности по сравнению с данными животных, получавших диклофенак натрия и ПСП раздельно. Уровень лейкоцитов и СОЭ был сопоставим с показателями животных, получавших диклофенак натрия.
У интактных животных содержание МДА в лизате эритроцитов составило 8,48 ± 1,06 нмоль/мг белка, тиоловых групп – 154,14 ± 44,8 мкмоль/мг белка, активность GST – 1,24 ± 0,19 нмоль ХДБН/мин∙мг белка, GPх – 2,90 ± 0,43 нмоль НАДФ/мин∙мг белка.
У контрольных животных через 4 часа после введения флогогенного агента уровень МДА в гемолизате эритроцитов увеличился на 35,29 % (р < 0,05), активность GST повысилась на 27,41 % (р ˃ 0,05), содержание тиоловых групп снизилось на 19,41 % (р < 0,05), активность GPх – на 50,69 % (р ˃ 0,05) по сравнению с данными интактных животных (рисунок).
Таблица 1
Уровень лейкоцитов и СОЭ у крыс с экспериментальным воспалением
|
Серия животных (n = 7) |
Время после введения флогогенного агента |
Уровень лейкоцитов |
СОЭ |
|
Интактные животные |
11391,7 ± 292,0 |
1,5 ± 0,2 |
|
|
Контрольная группа |
4 ч 3 сут 7 сут |
34967,7 ± 793,7* 22557,0 ± 445,9* 15854,0 ± 154,7* |
1,7 ± 0,1 3,5 ± 0,1* 1,8 ± 0,1 |
|
ПСП |
4 ч 3 сут 7 сут |
21445,0 ± 145,6** 13667,8 ± 274,4** 11408,8 ± 222,7** |
1,6 ± 0,2 2,6 ± 0,1** 1,6 ± 0,1** |
|
Диклофенак натрия |
4 ч 3 сут 7 сут |
16509,1 ± 227,1** 14452,8 ± 338,8** 11742,1 ± 516,2** |
1,7 ± 0,1 2,2 ± 0,3** 1,4 ± 0,1** |
|
Комбинация ПСП + диклофенак натрия |
4 ч 3 сут 7 сут |
16431,4 ± 133,8** 13943,9 ± 164,1** 12101,7 ± 788,9** |
1,6 ± 0,1 2,5 ± 0,1** 1,4 ± 0,1** |
Примечания: * – р < 0,05 – сравнение с интактными животными; ** – р < 0,05 – сравнение с контролем патологии.
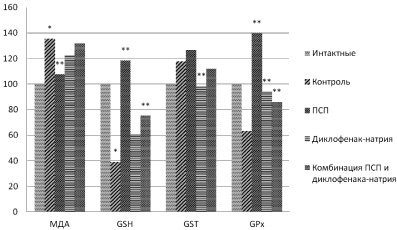
Содержание (в процентах от нормы) МДА, тиоловых групп и ферментов в гемолизате эритроцитов через 4 часа после моделирования отека у животных контрольной серии и на фоне лечения. Примечания: р < 0,05* – сравнение с интактными животными, р < 0,05** – сравнение с контролем патологии
Содержание МДА в гемолизате эритроцитов у крыс, получавших ПСП, через 4 часа после введения формалина снизилось на 40,43 % (р < 0,05), содержание безбелковых тиоловых групп увеличилось на 202,57 % (р < 0,05), активность GST повысилась на 6,33 % (р > 0,05) и GPх на 127,97 % (р < 0,05). При сравнении полученных результатов с данными интактных животных выявлена нормализация уровня МДА и безбелковых тиоловых групп, активность GST и GPх увеличилась на 35,48 и 12,41 % соответственно, что можно расценивать как стимуляцию системы антиоксидантной защиты клетки.
Уровень МДА в гемолизате эритроцитов крыс, получавших диклофенак натрия, через 4 часа после введения формалина не изменялся, содержание тиоловых групп увеличилось на 39,97 % (р ˃ 0,05), активность GST снизилась на 22,78 % (р < 0,05), GP – повысилась на 56,64 % (р < 0,05) по отношению к контролю патологии. При сравнении результатов данной серии с показателями интактных крыс наблюдалось достоверное (р < 0,05) повышение уровня МДА на 22,35 % и снижение содержания безбелковых тиоловых групп на 45,23 %, активность GST и GPх была снижена (р ˃ 0,05). Полученные результаты характеризуют прооксидантное действие диклофенака в раннем периоде воспалительной реакции.
При совместном введении ПСП и диклофенака через 4 часа после инъекции флогогенного агента уровень МДА не менялся, содержание тиоловых групп возросло на 92,15 % (р < 0,05), активность GPх повысилась на 36,00 % (р < 0,05), GST – не изменилась по отношению к контролю. По сравнению с данными интактных животных отмечалось достоверное (р < 0,05) повышение уровня МДА на 31,92 %, снижение содержания безбелковых тиоловых групп на 24,84 %, активность GST повышалась (р > 0,05), а GPх снижалась (р > 0,05).
На 7 сутки исследования как в контроле патологии, так и во всех сериях лечения экспериментального отека, изменений показателей ПОЛ и системы антиоксидантной защиты по сравнению с данными интактных животных выявлено не было.
Антиоксидантная активность ПСП связана, видимо, с активацией ферментов, отвечающих за распад перекисных соединений, образующихся в ходе воспалительной реакции. Наличие в молекуле ПСП свободных карбоксильных и гидроксильных групп позволяет связывать свободные радикалы. Кроме того, полисахаридный комплекс является поверхностно-активным веществом и способен образовывать защитный слой на поверхности молекул, взаимодействуя с гликопротеинами и протеогликанами гликокаликса [5, 8].
В эксперименте по изучению противоязвенной активности ПСП получены результаты, представленные в табл. 2. Двукратное введение индометацина в дозе 20 мг/кг массы приводило к образованию эрозивно-язвенных повреждений у 100 % животных всех групп. При макроскопическом исследовании желудка крыс контрольной группы деструкции дифференцировали на крупные (7,43 ± 4,79), полосовидные (5,00 ± 3,27) и точечные (10,71 ± 2,93), индекс Паулса составил 23,14.
Таблица 2
Влияние ПСП, омепразола и ранитидина на развитие эрозивно-язвенных поражений, вызванных введением индометацина
|
Группа животных (n = 7) |
Количество деструкций на 1 животное |
Индекс Паулса |
Противоязвенная активность |
||
|
Крупные |
Полосовидные |
Точечные |
|||
|
Контроль |
7,43 ± 4,79 |
5,00 ± 3,27 |
10,71 ± 2,93 |
23,14 |
|
|
ПСП |
3,00 ± 1,63* |
0,00 (0,00;0,00) ** |
6,71 ± 1,49* |
10,00 |
2,31 |
|
Ранитидин |
2,00 (0,00;2,00)* |
0,00 (0,00;3,00)* |
8,14 ± 2,91 |
10,29 |
2,25 |
|
Омепразол |
1,14 ± 1,21* |
0,00 (0,00;0,00) ** |
7,57 ± 1,99* |
9,28 |
2,49 |
Примечания: * – р < 0,05, ** – р < 0,005 по сравнению с контролем.
У животных, получавших ПСП, количество деструкций достоверно снижалось по сравнению с данными контроля: количество крупных язв уменьшилось в 2,48 раза (р < 0,05), точечных – в 1,6 раза (р < 0,05), полосовидные язвы присутствовали у одного животного. Противоязвенная активность ПСП составила 2,31, что свидетельствует о выраженном гастропротекторном эффекте ПСП при профилактическом приеме.
У животных, получавших препараты сравнения – омепразол и ранитидин, также отмечено значительное снижение количества деструкций. Введение ранитидина уменьшало образование крупных изъязвлений в 3,72 раз (р < 0,05), омепразола – в 6,52 раза (р < 0,05). Полосовидные язвы при введении ранитидина обнаружены у двух животных, при введении омепразола – у одного. Число точечных деструкций достоверно снижалось в 1,41 раза при введении омепразола, при назначении ранитидина данный показатель уменьшился недостоверно. Противоязвенная активность ранитидина составила 2,25; омепразола – 2,49.
Полученные результаты свидетельствуют, что ПСП уступает антисекреторным препаратам по предупреждению возникновения крупных язв, однако сопоставим по профилактике полосовидных и точечных язв. Сравнительный анализ по коэффициенту противоязвенной активности позволяет представить следующий ряд сравнительной эффективности исследуемых веществ: ранитидин < ПСП < омепразол.
Гастропротекторное действие ПСП, возможно, обусловлено его поверхностно-активными свойствами, обволакивающим действием, образованием защитной пленки на поверхности язв, а также стимуляцией регенерации слизистой оболочки желудка.
Выводы
1. Воспалительная реакция, вызванная введением формалина под апоневроз стопы крыс, сопровождается развитием системного окислительного стресса, повышением концентрации МДА, снижением содержания безбелковых тиоловых групп и активацией глутатионтрансферазы в лизате эритроцитов.
2. Полисахаридный комплекс цветков пижмы обыкновенной при пероральном введении в дозе 0,3 г/кг массы курсом 7 дней оказывает выраженное тормозящее действие на развитие экссудативного компонента воспалительной реакции, снижает лейкоцитоз и уровень СОЭ. Противовоспалительная активность полисахарида сравнима с диклофенаком натрия.
3. Полисахарид цветков пижмы обыкновенной проявляет выраженное антиоксидантное действие, вызывая снижение концентрации МДА, повышение содержания безбелковых тиоловых групп и активности глутатионпероксидазы в раннем периоде оксидативного стресса, вызванного воспалительной реакцией.
4. Одновременное введение полисахарида пижмы обыкновенной и диклофенака натрия существенно не меняет динамику развития отека конечности, количество лейкоцитов и СОЭ, однако повышает уровень антиоксидантной защиты, уменьшая прооксидантное действие диклофенака в раннем периоде воспалительной реакции.
5. Полисахаридный комплекс цветков пижмы обыкновенной при профилактическом введении в дозе 0,3 г/кг массы в течение 4-х дней оказывает выраженное гастропротекторное действие, снижая количество деструктивных эрозивно-язвенных поражений, вызванных введением индометацина. Противоязвенная активность полисахарида в эксперименте превосходит эффективность ранитидина и сравнима с омепразолом.
Рецензенты:
Филиппенко Н.Г., д.м.н., профессор, зав. каф. клинической фармакологии, ГБОУ ВПО КГМУ Минздрава России, г. Курск;
Ушкалова Е.А., д.м.н., профессор, кафедры общей и клинической фармакологии медицинского факультета, ФГБОУ ВПО «Российский университет дружбы народов», г. Москва.
Работа поступила в редакцию 23.07.2014.
Библиографическая ссылка
Якушева Е.Н., Сычев И.А., Кириченко Е.Е., Щулькин А.В. ИЗУЧЕНИЕ ФАРМАКОЛОГИЧЕСКОЙ АКТИВНОСТИ ПОЛИСАХАРИДНОГО КОМПЛЕКСА ЦВЕТКОВ ПИЖМЫ ОБЫКНОВЕННОЙ // Фундаментальные исследования. 2014. № 7-5. С. 1070-1074;URL: https://fundamental-research.ru/ru/article/view?id=34831 (дата обращения: 31.05.2026).



