Адеметионин (S-аденозил-L-метионин) играет важную роль в биохимических процессах в организме человека. Он участвует в реакциях трансметилирования, является предшественником цистеина, таурина, глутатиона. Применяется адеметионин при внутрипеченочном холестазе, токсическом поражении печени, в том числе алкогольном, лекарственном, при вирусном гепатите и т.п. Адеметионин вырабатывается клетками печени. Однако при некоторых заболеваниях печени требуется принимать дополнительно адеметионин в качестве лекарственного средства [1].
В настоящее время субстанция адеметионина в РФ не производится.
Нами поставлена цель изучить существующие способы и разработать наиболее доступный способ получения адеметионина.
Описанные в литературе способы получения адеметионина можно разделить на три группы.
Один из первых способов получения адеметионина, который разработал Д. Кантони, заключался в синтезе адеметионина из аденозинтрифосфата (АТФ) и метионина в присутствии очищенного печеночного фермента метионинаденозилтрансферазы. В настоящее время метод не применяется из-за сложности выделения и очистки фермента [2].
Аналогичный метод получения адеметионина из АТФ и метионина отличается лишь тем, что метионинаденозилтрансферазу получают из дрожжевого экстракта. Этот метод также требует выделения и очистки фермента.
Ко второй группе методов можно отнести синтез адеметионина путем метилирования S-аденозил-L-гомоцистеина. Варианты такого синтеза различаются метилирующими агентами. Однако эти методы оказались непригодными, так как в результате синтеза образуется неактивный S,Rизомер и лишь небольшая часть активного S,S-изомера. Помимо этого указанный метод дает большое количество примесей из-за возможностей метилирования разных реакционных центров S-аденозил-L-гомоцистеина [3].
С практической точки зрения наиболее успешными оказались методы биосинтеза адеметионина. Сущность метода заключается в накоплении адеметионина в дрожжевых клетках в питательной среде, обогащенной метионином, лизисе дрожжевых клеток и выделении адеметионина [4, 5].
Нами изучена возможность получения адеметионина методом биосинтеза.
В качестве продуцента адеметионина мы использовали Saccharomyces сerevisiae, а в качестве питательной среды была выбрана среда Шленка.
Дрожжи культивировали в течение 24–30 часов при постоянном перемешивании и аэрации при температуре 30 °С. Затем проводили лизис дрожжей, содержащих адеметионин, с помощью органического растворителя и разбавленной кислоты серной. В качестве органического растворителя нами был использован этилацетат, а оптимальной концентрацией серной кислоты оказалась концентрация от 0,05 до 0,2 моль/л. Время проведения лизиса – 2 часа при постоянном перемешивании. Экстракция данным способом позволяет получить практически 100 % адеметионина, присутствующего в дрожжах. Полученный лизат отделяли от остатков дрожжей при помощи центрифугирования.
На следующей стадии осуществляли очистку лизата. Для этого адеметионин из лизата осаждали 10 % раствором пикролоновой кислоты в н-бутаноле, который добавляли при перемешивании к предварительно подкисленному до pH 2 лизату. Полученный осадок отстаивали в течение 12 часов, отфильтровывали и промывали дважды холодной водой.
На заключительной стадии получали стабильную соль адеметионина с толуолсульфокислотой.
К высушенному осадку пикролоната адеметионина добавляли при энергичном встряхивании растворы 0,1 моль/л серной и толуолсульфокислоты, органический растворитель – н-бутанол. Отстаивали в течение 20 минут, органический слой удаляли, водный слой промывали н-бутанолом до удаления следов пикролоновой кислоты. Затем к водному слою добавляли обесцвечивающий уголь, затем фильтровали.
К полученному бесцветному водному раствору добавляли этанол. Образующийся осадок отделяли декантацией и растворяли в метанольном растворе толуолсульфокислоты с концентрацией 15 %.
На заключительной стадии к полученному раствору добавляли хлороформ, который осаждает двойную соль адеметионина с серной и п-толуолсульфокислотой.
Полученная таким образом соль адеметионина представляет собой гигроскопичный порошок, очень легко растворимый в воде, практически нерастворимый в этаноле, ацетоне и других органических растворителях.
Для уменьшения гигроскопичности к полученной субстанции добавляли лактозу в соотношении 1:1.
Методом УФ-спектроскопии была подтверждена подлинность полученной соли а также установлен количественный состав компонентов.
УФ-спектроскопию использовали для идентификации полученной соли. Водный раствор соли в области от 200 до 300 нм должен иметь 2 максимума, соответствующих адеметионину 258 ± 2 нм и п-толуолсульфокислоте 230 ± 2 нм.
Для этого точную навеску полученной соли (около 0,2 г) помещали в мерную колбу вместимостью 100 мл, прибавляли 50 мл воды, растворяли и доводили тем же растворителем содержимое колбы до метки. Аликвоту в количестве 1 мл переносили в мерную колбу вместимостью 100 мл, доводили водой до метки и регистрировали спектр поглощения в области от 220 до 300 нм (рис. 1).
Как видно из рис. 1, в спектре поглощения раствора испытуемого образца имеются 2 максимума при длинах волн 231 нм (п-толуолсульфокислота) и 256 нм (адеметионин).
Для количественного определения компонентов нами разработана спектрофотометрическая методика.
На первом этапе исследований нами была приготовлена модельная смесь адеметионина с п-толуолсульфокислотой с целью определения возможности использования непосредственного спектрофотометрического метода.
На рис. 2 представлен спектр поглощения модельной смеси, содержащей адеметионин и п-толуолсульфокислоту.
Из приведенного спектра видно, что полосы поглощения веществ перекрываются и делают невозможным непосредственное спектрофотометрическое определение адеметионина и п-толуолсульфокислоты. Поэтому для определения их содержания нами был использован метод Фирордта. На основании полученного спектра поглощения были выбраны аналитические длины волн. Готовили 6 модельных смесей адеметионина и п-толуолсульфокислоты, для которых аналитические длины волн были равны λ1 = 231 нм и λ2 = 256 нм.
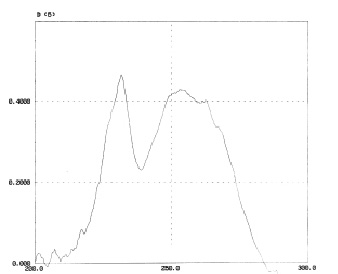
Рис. 1. Спектр поглощения раствора соли адеметионина с п-толуолсульфокислотой
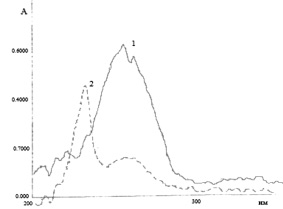
Рис. 2. Спектр поглощения модельной смеси, содержащей адеметионин и п-толуолсульфокислоту
Точную навеску модельной смеси (около 0,1 г) растворяли в мерной колбе вместимостью 100 мл в 50 мл воды, доводили раствор в колбе до метки тем же растворителем. Аликвоту в количестве 5 мл переносили в мерную колбу вместимостью 100 мл, доводили объем раствора до метки водой. Оптическую плотность раствора измеряли при длинах волн 231 и 256 нм. Раствор сравнения – вода.
Для расчёта каждого компонента в смеси определяли удельный показатель поглощения при длинах волн 231 и 256 нм.
Таблица 1
Значение удельных показателей поглощения при аналитических длинах волн
|
Название лекарственного вещества |
λ = 256 нм |
λ = 231 нм |
|
Адеметионин |
84,09 |
23,86 |
|
11,2 |
19,94 |
Расчет содержания каждого компонента в образцах проводили путем решения системы уравнений
А1 = Х1Е11 + Х2Е12
А2 = Х1Е21 + Х2Е22
Таким же образом было проведено определение компонентов в соли адеметионина с серной и п-толуолсульфокислотой.
Таблица 2
Результаты определения адеметионина и п-толуолсульфокислоты в модельной смеси
|
Взято адеметионина |
Найдено адеметионина |
Взято п-толуолсульфокислоты |
Найдено п-толуолсульфокислоты |
||
|
г |
% |
г |
% |
||
|
0,01126 |
0,01130 |
100,36 |
0,09581 |
0,03529 |
99,72 |
|
0,01142 |
0,01120 |
98,07 |
0,09927 |
0,03518 |
99,07 |
|
0,01079 |
0,01106 |
102,50 |
0,10032 |
0,03524 |
99,04 |
|
0,01158 |
0,01150 |
99,31 |
0,09647 |
0,03528 |
99,49 |
|
0,01135 |
0,01133 |
97,82 |
0,09754 |
0,03517 |
99,12 |
|
0,01145 |
0,01146 |
100,09 |
0,09687 |
0,03571 |
100,90 |
|
Метрологические характеристики
SD = 0,5181 RSD = 0,5194
|
Метрологические характеристики
SD = 0,7251 RSD = 0,7281
|
||||
Результаты определения приведены в табл. 3.
Таблица 3
Результаты анализа двойной соли
|
Наименование соли |
Найдено вещества, % |
|
Адеметионин П-толуолсульфокислота |
40,0 ± 0,9 50,0 ± 1,0 |
Приведенные результаты показывают, что методика определения соли адеметионина с серной и п-толуолсульфокислотой позволяет определить все компоненты с погрешностью не более 3 %.
Выводы
1. Разработан биосинтетический способ получения двойной соли адеметионина.
2. Разработаны спектрофотометрические методики подлинности двойной соли адеметионина с серной и п-толуолсульфокислотой.
3. Разработаны методики количественного определения компонентов двойной соли при помощи метода Фирордта.
Рецензенты:
Лазарян Д.С., д.фарм.н., профессор, заведующий кафедрой фармацевтической химии Пятигорского медико-фармацевтического института, филиала ГБОУ ВПО ВолгГМУ, г. Пятигорск;
Кодониди И.П., д.фарм.н., доцент кафедры органической химии Пятигорского медико-фармацевтического института, филиала ГБОУ ВПО ВолгГМУ, г. Пятигорск.
Работа поступила в редакцию 25.12.2013.
Библиографическая ссылка
Морозов А.В. РАЗРАБОТКА СПОСОБА ПОЛУЧЕНИЯ ДВОЙНОЙ СОЛИ АДЕМЕТИОНИНА С СЕРНОЙ И П-ТОЛУОЛСУЛЬФОКИСЛОТОЙ // Фундаментальные исследования. 2013. № 11-6. С. 1203-1206;URL: https://fundamental-research.ru/ru/article/view?id=33277 (дата обращения: 02.05.2026).




 = 99,75
= 99,75
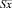 = 0,2115
= 0,2115
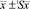 = 99,75 ± 0,5438
= 99,75 ± 0,5438
 = 99,59
= 99,59
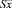 = 0,2960
= 0,2960
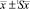 = 99,59 ± 0,7610
= 99,59 ± 0,7610