По данным Всемирной организации здравоохранения, жертвами туберкулеза ежегодно становятся порядка 1,7 миллионов и ежедневно умирают около 5 тысяч человек. Происходит быстрое распространение лекарственно-устойчивой формы туберкулеза. В отчете ВОЗ «Глобальный доклад 2010 года об эпидемическом надзоре и ответных действиях» от 18 марта 2010 г., особое внимание уделяется росту заболеваемости множественным лекарственноустойчивым туберкулезом [9].
По данным ВОЗ, в некоторых районах мира у каждого четвертого человека с туберкулезом развивается форма болезни, которая не поддается стандартному лечению противотуберкулезными препаратами первой линии. В настоящее время к странам, где наблюдается высокий уровень заболеваемостью туберкулезом с приобретенной множественной и широкой лекарственной устойчивостью, относятся и страны СНГ, в том числе Россия и Казахстан.
Крайне неблагоприятная ситуация складывается в отношении лечения детей, больных туберкулезом, поскольку в мире ранее не выпускались специальные лекарственные формы для детей. В основном для лечения детей использовались лекарственные препараты, предназначенные для взрослых. В этих случаях таблетки размалывали и расфасовывали в соответствующих дозах. В большинстве случаев это приводило к снижению терапевтической активности лекарственных препаратов и проявлению ряда побочных эффектов[9, 10].
В декабре 2007 года ВОЗ была объявлена глобальная кампания по производству лекарственных средств для детей, вызванная необходимостью улучшения доступа к безопасным лекарствам для всех детей в возрасте до 15 лет. Оптимальными для детей лекарственными препаратами являются адаптируемые твердые оральные формы, предпочтительно диспергируемые таблетки [3].
Фармацевтической компанией «РОМАТ», Казахстан, разработан состав и технология нового детского лекарственного препарата – Изониазид-Д (диспергируемые таблетки) на основе инкапсулирования изониазида с β-циклодекстрином для снижения токсичности, маскировки неприятного вкуса и повышения стабильности при хранении противотуберкулезного препарата изониазида [2].
Создание воспроизведенных лекарственных препаратов (дженериков) предполагает обязательное проведение фармакокинетических исследований, оценку их биоэквивалентности оригинальному лекарственному препарату, что является основным видом медико-биологического контроля их качества [1, 5].
Исходя из сказанного, целью настоящей работы явилось изучение относительной биодоступности Изониазида-Д таблетки диспергируемые производства ТОО «Павлодарский фармацевтический завод», Республика Казахстан, в сравнении с лекарственным препаратом Изониазид таблетки диспергируемые (Кадила Фармасьютикалс Лтд, Индия).
Материалы и методы исследования
Изониазид – противотуберкулезный препарат первого ряда, производное гидразида изоникотиновой кислоты (гидразид 4-пиридинкарбоновой кислоты).
Тестируемый препарат – таблетки диспергируемые изониазид 0,1 г производства ТОО «Павлодарский фармацевтический завод», Республика Казахстан. В качестве препарата-сравнения выбран аналог, не зарегистрированный в Республике Казахстан – таблетки диспергируемые 0,1 г производства Кадила Фармасьютикалс Лтд, Индия, так как на фармацевтическом рынке Казахстана отсутствует аналог тестируемого препарата по лекарственной форме и дозировке.
Исследование проводилось на кролика-самцах породы Шиншилла массой тела – 3,19 ± 0,41 кг, полученных из питомника ТОО НПП «Антиген» (г. Алматы).
В «случайном» порядке животным с помощью зонда внутрь вводили 1 таблетку испытуемого лекарственного препарата Изониазида-Д таблетки диспергируемые 0,1 (Т) или 1 таблетку препарата сравнения Изониазид таблетки диспергируемые 0,1 (R). Промежуточный период составил 7 дней, по истечении которого препараты вводили в обратном порядке.
Образцы крови (около 1,0 мл) отбирали из краевой ушной вены с помощью игл и переносили в центрифужные пробирки, предварительно обработанные гепарином. Взятие образцов крови для последующего определения содержания препарата в плазме крови осуществлялось в дискретные интервалы времени: через 0; 0,5; 1,0; 2,0; 3,0; 4,0; 6,0; 8,0; 12,0 и 24,0 часа после их перорального введения. Образцы крови отстаивались в течение 15 минут в условиях комнатной температуры. После центрифугирования (3000 об/мин в течение 10 минут) отбирали плазму крови, которая хранилась при температуре –30 °С в морозильной камере «Premium».
Для количественного определения изониазида в плазме крови использовали хроматографический метод [4]. Анализ проводили на жидкостном хроматографе «Agilent 1100» с УФ-детектором и компьютером с соответствующим пакетом программ для обсчета результатов. Условия хроматографирования: аналитическая колонка – «Zorbax Bonus-RP», Agilent (150´4,6 мм; 5 мкм); подвижная фаза: градиент растворителей А и В, профильтрованная через мембранный фильтр с размером пор 0,45 мкм и дегазированная на ультразвуковой бане; скорость потока элюента – 1,0 мл/мин; детектирование проводили при длине волны – 280 нм; температура колонки + 35 °С.
Для экстракции изониазида из плазмы крови 0,5 мл плазмы помещали в пробирку Centrisart I и центрифугировали в течение 15 мин при 4500 об/мин. По 50 мкл надосадочной жидкости вводили в петлю инжектора. Процент извлечения изониазида составил 84,6 % ± 6,7 (среднее из 3 определений). В диапазоне концентраций 10; 25; 50 и 100 мкг/мл калибровочная зависимость была линейной.
Количественное определение изониазида проводили методом абсолютной калибровки. В описанных условиях время удерживания изониазида составило 3,25–4,33 мин. В диапазоне концентраций 10–100 мкг/мл калибровочная кривая была линейной. Стандартная кривая изониазида описывалась уравнением: y = 46,756x + 178,42 (R2 = 0,9636), где y – площадь хроматографического пика изониазида; х – концентрация в мкг/мл. Минимальная обнаруживаемая концентрация составила 0,01 мкг/мл; относительная ошибка для концентрации 100 мкг/мл не более 32,8 %.
Полученные данные предварительно были подвергнуты математической статистической обработке с помощью программы «Excel». Расчет фармакокинетических параметров анализируемых препаратов был проведен с использованием программы «ANOVA».
Результаты исследования и их обсуждение
С целью оценки биологической доступности исследуемых лекарственных средств были определены концентрации изониазида в сыворотке крови кроликов: рассчитаны основные фармакокинетические параметры, позволяющие количественно охарактеризовать относительную биодоступность (f), величины площадей под фармакокинетическими кривыми зависимости «концентрация-время» (AUC0-360), время достижения максимальной концентрации (Тmax) и значения максимальных концентраций (Сmax) [1, 7].
На рисунке представлен усредненный фармакокинетический профиль изониазида после введения тестируемого и референс-препаратов.
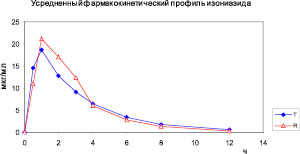
Усредненный фармакокинетический профиль изониазида в плазме крови кроликов после однократного перорального введения Изониазида-Д (Т) и Изониазида (R)
Профили концентраций изониазида препаратов Изониазид-Д (T) и Изониазид (R) схожи. Фармакокинетические кривые изониазида показывают, что исследуемое соединение определяется на протяжении 12 часов после однократного введения животным испытуемого препарата и препарата сравнения.
В табл. 1 представлены фармакокинетические параметры изониазида у кроликов после введения исследуемых препаратов.
Таблица 1
Индивидуальные и средние значения фармакокинетических параметров изониазида тестируемого (Т) и референс-препаратов (R)
|
№ п/п |
tmax, ч |
Cmax, мкг/мл |
AUC0 → t, мкг/мл∙ч |
Cmax/AUC0 → t, ч–1 |
||||
|
T |
R |
T |
R |
T |
R |
T |
R |
|
|
1 |
1,00 |
1,00 |
26,56 |
28,09 |
89,97 |
78,39 |
0,295 |
0,358 |
|
2 |
0,50 |
1,00 |
9,81 |
10,91 |
26,79 |
40,15 |
0,366 |
0,272 |
|
3 |
1,00 |
2,00 |
20,43 |
21,31 |
49,08 |
67,80 |
0,416 |
0,314 |
|
4 |
1,00 |
1,00 |
27,00 |
26,96 |
96,78 |
104,95 |
0,279 |
0,257 |
|
5 |
2,00 |
1,00 |
20,82 |
25,57 |
70,03 |
72,88 |
0,297 |
0,351 |
|
6 |
0,50 |
0,50 |
23,11 |
25,27 |
62,01 |
57,07 |
0,373 |
0,443 |
|
x |
1,00 |
1,08 |
21,29 |
23,02 |
65,78 |
70,21 |
0,34 |
0,33 |
|
SD |
0,50 |
0,45 |
5,72 |
5,81 |
23,73 |
19,85 |
0,05 |
0,06 |
|
|
0,20 |
0,18 |
2,34 |
2,37 |
9,68 |
8,10 |
0,02 |
0,03 |
|
C.V., % |
50,00 |
41,42 |
26,88 |
25,23 |
36,07 |
28,27 |
14,86 |
18,58 |
Сравнительный анализ основных фармакокинетических параметров изониазида показал, что изучаемый препарат быстро всасывается в системный кровоток из желудочно-кишечного тракта. Значения Сmax/AUC0 ® t для препаратов Изониазид-Д и Изониазид статистически достоверно не различаются и составляют в среднем 0,34 ± 0,05 и 0,33 ± 0,06 ч–1 соответственно, а индивидуальный разброс значений – C.V. незначительный (14,86–18,58 %). Время достижения максимальной концентрации (Тmax) составило в среднем для Т–1,00 ± 0,50 и для R–1,08 ± 0,45 ч. Значения Тmax для тестируемого и референс-препаратов статистически достоверно не различаются. Приведенные данные свидетельствуют, что у исследуемых препаратов время достижения максимальной концентрации (Тmax) соответствует данным научной литературы [6, 8].
Средняя максимальная концентрация изониазида, определяемая в плазме крови кроликов (Сmax), для тестируемого препарата составила 21,29 ± 5,72 мкг/мл и для препарата-сравнения – 23,02 ± 5,81 мкг/мл. Изониазид быстро достигает максимальной концентрации и быстро выводится из организма: через 24 часа после введения обнаруживаются следовые концентрации в плазме крови кроликов.
Индивидуальный анализ основного параметра, характеризующего степень биодоступности действующего вещества из лекарственной формы – AUC0 → t указывает на значительную вариабельность данного параметра. Среднее значение AUC0 → t для тестируемого препарата составило 65,78 ± 23,73 и для R–70,21 ± 19,85 мкг/мл∙ч. Доверительные интервалы для логарифмически преобразованных значений AUC составляют от 3,29 до 4,57, а для логарифмически преобразованных значений Cmax – от 2,28 до 3,30 и не выходят за допустимые границы [6].
Относительная биологическая доступность (f) изониазида, определяемая отношением индивидуальных значений AUC0-t тестируемого препарата по отношению к референс-препарату, у всех кроликов находится в диапазоне 66,72–114,77 %, среднее значение составляет – 91,81 ± 17,49 % (табл. 2). Имел место незначительный разброс индивидуальных значений относительной биодоступности, коэффициент вариации составил 19,05 %.
Таблица 2
Индивидуальные значения относительной биодоступности (AUCT/AUCR) изониазида тестируемого (Т) и референс-препарата (R)
|
№ п/п |
AUCT/ AUCR |
|
1 |
114,77 |
|
2 |
66,72 |
|
3 |
72,39 |
|
4 |
92,22 |
|
5 |
96,09 |
|
6 |
108,66 |
|
x |
91,81 |
|
SD |
17,49 |
|
|
7,14 |
|
C.V. % |
19,05 |
Заключение
В результате исследований установлено, что после однократного введения испытуемого препарата – Изониазид-Д таблетки диспергируемые лекарственное средство изониазид достигает системного кровотока. При этом уровни максимальных концентраций изониазида в плазме крови животных после перорального введения испытуемого препарата и препарата сравнения сопоставимы друг с другом.
После введения исследуемых препаратов экспериментальным животным не выявлено достоверных различий в скорости всасывания (Cmax/AUC) и времени наступления максимальной концентрации изониазида в плазме крови. Относительная биодоступность исследуемого препарата по отношению к препарату сравнения в среднем составила 91,81 %.
Рецензенты:
Ефименко Н.В., д.м.н., профессор, Пятигорский государственный НИИ курортологии ФМБА России, г. Пятигорск;
Андреева И.Н., д.фарм.н., профессор кафедры туризма КМВИС, г. Пятигорск.
Работа поступила в редакцию 06.03.2014.
Библиографическая ссылка
Ким М.Е., Мурзагулова К.Б., Степанова Э.Ф. ИССЛЕДОВАНИЕ БИОДОСТУПНОСТИ ЛЕКАРСТВЕННОГО ПРЕПАРАТА ИЗОНИАЗИД-Д ТАБЛЕТКИ ДИСПЕРГИРУЕМЫЕ // Фундаментальные исследования. – 2014. – № 3-4. – С. 766-769;URL: https://fundamental-research.ru/ru/article/view?id=33752 (дата обращения: 19.04.2024).