Компьютерное моделирование поверхности потенциальной энергии (ППЭ) комплексов 2-метил-1,3,2-диоксаборинана - типичной кислоты Льюиса - с основаниями Льюиса - водой и аммиаком (1:1) методом RHF//AM1 показало, что возможны лишь несколько стабильных ассоциатов между одной молекулой основания и циклическим борным эфиром: два в случае воды и три в случае аммиака. Для всех типов комплексов на ППЭ выявлены основные и локальные минимумы и отдельные максимумы.
Решение основных задач конформационного анализа предполагает, как известно, определение стабильных конформеров и барьеров перехода между ними. Интерес к строению циклических эфиров борных кислот обусловлен электронными и стерическими внутримолекулярными взаимодействиями, вызванными присутствием электронодефицитного атома бора и электронодонорных гетероатомов кислорода в одной молекуле [1-3]. Поверхность потенциальной энергии (ППЭ) таких систем, согласно представленной ниже схеме конформационной изомеризации 2-метил-1,3,2-диоксаборинана, содержит минимум, отвечающий конформеру софы (С) и максимум, соответствующий 2,5-твист-форме (2,5-Т) [4,5].
![]()
В этой связи целью настоящей работы является компьютерное моделирование поверхности потенциальной энергии (ППЭ) 2-метил-1,3,2-диоксаборинана - типичной кислоты Льюиса - в присутствии оснований Льюиса - молекул воды и аммиака, осуществленное методом Хартри-Фока с помощью полуэмпирического приближения АМ1 в рамках программного обеспечения HyperChem [6].
Присутствие электронодонорных молекул, как и следовало ожидать, существенно меняет характер конформационных превращений борного эфира. Нами обнаружено, что в случае системы: одна молекулы воды - одна молекула 1,3,2-диоксаборинана - среди множества типов бинарных структур существует только два относительно стабильных ассоциата. Один из них содержит молекулу воды ориентированную практически симметрично относительно прямой, продолжающей биссектрису угла СОВ борного эфира (А), а другой представляет собой комплекс с координационной связью О→В (Б).
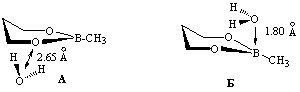
Обе системы характеризуются наличием двух практически вырожденных по энергии инвертомеров софы (А) либо искаженной софы (Б) (∆Е). Согласно расчетных данных энтальпии образования ∆Н наиболее устойчивым является ассоциат Б (табл.1). Длина связи О→В составляет 1.80 Å (по данным рентгеноструктурного анализа для ациклических молекул, содержащих четырехковалентный атом бора, соответствующее значение rB-O равно 1.45-1.60 Å [7,8]). Наблюдается также определенное увеличение длин эндоциклических связей В-О и связи В-С комплекса по сравнению с изолированной молекулой 2-метил-1,3,2-диоксаборинана. Еще одной важной характеристикой ППЭ обсуждаемой системы является заметное понижение потенциального барьера между двумя инвертомерами искаженной софы рассматриваемого ассоциата по сравнению с молекулами исходного борного эфира и комплекса А (∆Е≠).
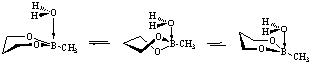
Таблица 1. Влияние молекулы воды на энергетические параметры инверсии цикла 2-метил-1,3,2-диоксаборинана (ккал/моль)
|
Соединение |
∆Н комплекса |
∆Е |
∆Е≠ |
|
Исходный борный эфир |
- |
0 |
3.2 |
|
А |
4.5 |
0 |
3.2 |
|
Б |
10.4 |
0.07 |
2.2 |
Остальные ассоциаты характеризуются более значительным расстоянием между атомом кислорода молекулы воды и ближайшим атомом борного эфира (от 3 до 7 Å); они на 9-10 ккал/моль менее устойчивы по сравнению с комплексом Б и по этой причине в настоящей работе не рассматриваются.
Молекула аммиака образует с борным эфиром несколько типов комплексов: с водородной связью N-H ··· O-B (В), ассоциат с молекулой аммиака, ориентированной вдоль биссектральной линии угла СОВ (Г) и с координационной связью N→B (Д).

При этом последний является наиболее устойчивым, а на ППЭ в этом случае помимо основного (К1) появляются промежуточные минимумы, отвечающие конформерам 1,4- и 2,5-твист-форм (1,4- и 2,5-Т) и кресла К2.
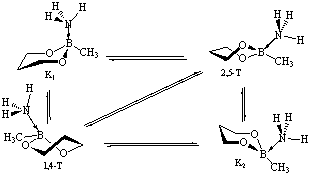
Расчетная длина координационной связи N→B (1.67 Å) близка к экспериментально наблюдаемой величине (1.57-1.64 Å [9,10]).
Представленная картина конформационных превращений уже не характерна для циклических эфиров борных кислот. Она аналогична ППЭ, наблюдаемой для молекул 1,3-диоксанов - ближайших циклических неборных аналогов 1,3,2-диоксаборинанов [11,12] - и свидетельствует о более глубоком, по сравнению с ассоциатом «борный эфир - вода», изменении конфигурации атома бора с тригональной на тетраэдрическую. Энергетические параметры ППЭ комплексов с аммиаком также свидетельствуют о заметном изменении относительной стабильности отдельных конформеров (табл.2).
Таблица 2. Энергетические параметры ППЭ ассоциатов аммиака с молекулой 2-метил-1,3,2-диоксаборинана (ккал/моль)
|
Комплекс |
∆Н |
Минимумы |
|||
|
К1 (С) |
К2 (С) |
1,4-Т |
2,5-Т |
||
|
В |
1.7 |
1.2 |
0 |
- |
- |
|
Г |
2.9 |
0 |
0 |
- |
- |
|
Д |
12.2 |
0 |
2.8 |
1.2 |
1.6 |
В результате конформационной изомеризации комплекса В образуется более стабильный ассоциат Г; инверсия цикла последнего идет между двумя вырожденными по энергии конформерами софы. Остальные ассоциаты характеризуются более значительным расстоянием между атомом азота молекулы аммиака и ближайшим атомом борного эфира (3-6 Å); они на 11-12 ккал/моль менее устойчивы по сравнению с комплексом Д и по этой причине в настоящей работе не рассматриваются.
Полученные результаты указывают на заметное влияние электронодонорных соединений на характер ППЭ молекул циклических борных эфиров и позволяют перейти к более детальному моделированию взаимодействий между молекулой 1,3,2 - диоксаборинана и несколькими молекулами электронодонорного соединения, выступающего в качестве растворителя.
СПИСОК ЛИТЕРАТУРЫ
- Грень А.И., Кузнецов В.В. Химия циклических эфиров борных кислот. Киев: Наукова думка, 1988. - 160 с.
- Кузнецов В.В. Автореф. дисс. докт. хим. наук. Уфа, 2002. - 47 с.
- Rossi K., Pihlaya K. // Acta Chem. Scand. - 1985. - V.B 39, N 8. - P.671.
- Валиахметова О.Ю., Бочкор С.А., Кузнецов В.В. // Баш. хим. журн. - 2004. - Т. 11, №1 . - С.79.
- Кузнецов В.В., Новиков А.Н. // Химия гетероцикл. соединений. - 2003. - №2. - С.295.
- HyperChem 7.01. Trial version. http://www.hyper.com/.
- Звиедре И.И., Марданенко В.К. // Изв. АН Латв. ССР. Сер. хим. - 1980. - №4. - С.495.
- Cotton F., Lisley W. // Inorg. Chem. - 1982. - V.21, -№ 1. - P.300.
- Ниденцу К., Даусон Д. Химия боразотных соединений. - М.: Мир, 1968. - 235 с.
- Hess H. // Acta Crystallogr. B. - 1969. - V.25, № 11. - P.2338.
- Курамшина А.Е., Бочкор С.А., Кузнецов В.В. // Баш. хим. журн. - 2004. - Т.11 , № 1. - С.81.
- Мазитова Е.Г., Курамшина А.Е., Кузнецов В.В. // Журн. орг. химии. - Т.40, вып. 4. - С.615.



