Несмотря на заметный прогресс, совершенствование технологии оказания медицинской помощи, ишемическая болезнь сердца продолжает оставаться ведущей причиной смертности населения большинства стран [2]. В диагностике заболеваний миокарда, и в частности, – коронарного атеросклероза последнее время придается значение контрастированной магнитно-резонансной томографии (МРТ) сердца, позволяющей наиболее точно дифференцировать необратимо поврежденный и жизнеспособный миокард [3]. Продолжает совершенствоваться и сама технология МР-коронароангиографии (МРКА), причем считается, что принципиальных препятствий к достижению визуализации коронарных артерий средствами МРКА нет [6]. При этом сегодня весь комплекс разработанных кардиологических методик и импульсных последовательностей МРТ для исследования сердца доступен как на высокопольных, так и средне-, и низкопольных МР-томографах с напряженностью поля от 0,2 Т и выше.
Наименее развитым разделом разработки новых диагностических технологий средствами МРТ в клинике коронарных атеросклеротических поражений остается исследование возможностей контрастированной МРТ в визуализации собственно коронарных атеросклеротических бляшек [9, 10]. На сегодня клинические исследования состояния коронарных бляшек средствами МРТ не проводятся даже при наличии в России немалого количества высокопольных МР-томографов, что обусловлено методическими трудностями, зачастую артефактами, вызванными движением сердца и аритмиями, а также большой «кривизной» хода коронарных артерий.
Между тем для относительно неподвижных в момент исследования атеросклеротических поражений периферических сосудов, в первую очередь каротидных и бедренных артерий, к настоящему времени достигнуты существенные успехи в визуализации их средствами контрастированной МРТ. Так, показана возможность надежной визуализации структур атеросклеротической бляшки с помощью контрастированной МРТ [11] и доказана взаимосвязь между степенью интенсивности контрастирования и риском развития ишемических цереброваскулярных повреждений [1]. Сходные данные в последнее время получены и для случая атеросклероза бедренных артерий [8]. Визуализация бляшек в этих случаях, как правило, осуществляется в традиционном Т1-взвешенном режиме, без дополнительных импульсных последовательностей типа «инверсия – восстановление». В кардиологических же исследованиях последовательность inversion – recovery является самой популярной и практически вытесняет из повседневной практики обычные Т1-взвешенные спин-эхо или турбо-спин-эхо изображения, поскольку за счет подбора времени инверсии позволяет значимо увеличить отношение интенсивностей накапливающего контраст поврежденного миокарда и сохранного, интенсивность которого стремятся приблизить к нулю. При этом внемиокардиальное накопление парамагнетика просто игнорируется.
Поэтому мы провели пилотное исследование возможности контрастирования атеросклеротических поражений коронарных артерий при проведении исследования на открытых МР-томографах у лиц с тяжелым коронарным атеросклерозом, перенесших острый инфаркт миокарда.
Материалы и методы исследования
В исследование были включены 22 пациента (20 мужчин, 2 женщины, средний возраст 61 ± 6 лет) с коронарным атеросклерозом, перенесших в прошлом (в течение 6 недель – полугода, в среднем 2,5 ± 1,1 мес) острый инфаркт миокарда, в том числе у 10 – в бассейне правой коронарной артерии (ПКА) при правом типе кровоснабжения, и у 12 – в бассейне огибающей ветви левой коронарной артерии (ЛКА). У всех инфаркт сопровождался подъемом сегмента ST; был осуществлен догоспитальный тромболизис без баллонирования и установки коронарного стента. При обследовании фракция выброса левого желудочка составляла 48 ± 9 % и не различалась достоверно между пациентами с поражением в бассейнах ПКА и ЛКА. Во всех случаях объем инфаркта миокарда по данным контрастированной МРТ не превышал 20 % массы миокарда ЛЖ. В группе пациентов с повреждением бассейна ЛКА у 5 из 12 пациентов отмечалась митральная регургитация, носившая минимальный характер и не сопровождавшаяся дилатацией предсердия. Пациенты с перенесенным инфарктом миокарда в бассейне передней нисходящей ветви ЛКА в данное исследование не включались, поскольку в предварительных исследованиях при анатомическом расположении атеросклеротического стенозирования в этой артерии относительно большим было влияние артефактов от эпикардиального жира. В последующем всем им выполнялось успешное аортокоронарное шунтирование, в среднем 3,6 ± 1,1 артерий.
В качестве лиц контрольной группы были взяты 8 пациентов сходного возраста (57 ± 8 лет), которым контрастированное исследование грудной клетки с ЭКГ-синхронизацией выполнялось по поводу предполагаемых опухолевых поражений, при этом клинической симптоматики ИБС у них не отмечалось.
Методики МР-томографии. Исследования были проведены на открытых МР-томографах (Аз-360, индукция поля 0,38Т, производства НПФ Аз и Magnetom Open, индукция поля 0,22Т производства Siemens). Исследования миокарда проводились в режиме Т1- взвешенных спин-эхо изображений, с ЭКГ-синхронизацией и получением изображений всего сердца в конечно-диастолический момент времени.
При этом изображения были получены в аксиальной плоскости (в 4-камерной позиции); параметры составляли соответственно TR = 450–890 мс (тем выше, чем реже ритм сердца пациента), TE = 15–25 мс, размер матрицы во всех случаях был 256×256, тогда как толщина среза 7–8 мм, а размер зоны исследования – до 25–29 см, т.е. с полным охватом анатомической области сердечной мышцы с размером вокселя до 0,1–0,12 мм. Такие размеры вокселя позволяют с достаточной уверенностью оценивать состояние анатомических структур, составляющих 3–7 мм.
Исследования выполнялись первоначально в состоянии покоя, а затем спустя 5–15 мин после внутривенного введения контрастного препарата-парамагнетика, что соответствует оптимальному времени накопления парамагнетика для «отсроченного» скана. При этом контрастный препарат – парамагнетик вводился в стандартной для кардиологических исследований миокарда дозе в 2 мл парамагнетика на 10 кг веса тела пациента. Технические параметры исследований до и после введения контраста-парамагнетика были неизменными.
Количественная и статистическая обработка результатов. Первоначально картина исходной и контрастированной МРТ сердца в Т1-взвешенном спин-эхо режиме оценивалась визуально, а затем выделялись области расположения проксимальных участков коронарных артерий, как правило, на уровне срезов, отстоящих не далее 0,8–1,6 см от уровня корня аорты – полулунных клапанов (рис. 1). Для сканов, записанных до и после контрастирования, средствами обработки изображений обводились области стенки коронарной артерии, и определялась интенсивность (яркость) изображения на воксель, в аппаратных единицах данного томографа. Оценка осуществлялась как на стороне инфаркт-связанной артерии, так и на противоположной, для области собственно бляшки и вне бляшки по ходу стенки артерии. На непораженной стороне при этом бляшка как таковая не выделялась. Затем рассчитывался индекс усиления интенсивности изображения как отношение
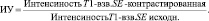
Сравнение величин ИУ проводилось между группами пациентов с поражением ЛКА, ПКА и контрольных лиц с использованием параметрического критерия Стьюдента для парных и непарных выборок, исходя из того, что он, как параметрический, является наиболее строгим в оценке межгрупповых различий.
Результаты исследования и их обсуждение
При визуальном анализе картины МРТ у пациентов с коронарным атеросклерозом (рис. 1, 2), во всех случаях удавалось уверенно визуализировать область расположения коронарных артерий по ходу их проксимальных участков, на протяжении до 3 см, с выделением области расположения стенозирования.
а 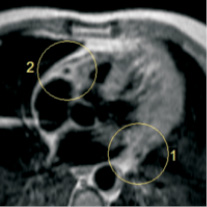 б
б 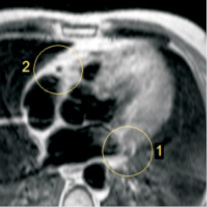
Рис. 1. Т1-взвешенная МР-томограмма патологических структур при атеросклерозе коронарных артерий и перенесенном инфаркте миокарда с контрастированием. Срезы в четырехкамерной позиции по длинной оси на уровне устьев коронарных артерий (а – до контраста, б – после). Отмечается накопление контраста в области стенозированных левой коронарной артерии (1) и правой коронарной артерии (2), по сравнению с доконтрастным исходным сканом (а)
а 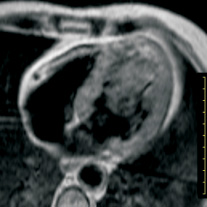 б
б 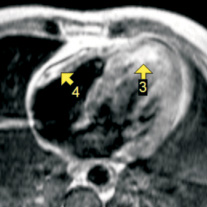
Рис. 2. На срезе МР-томограммы, полученной после контрастирования на уровне середины левого желудочка, визуализируется контрастное накопление в области перенесенного передне-перегородочного трансмурального инфаркта ЛЖ (стрелка 3), а также по ходу бляшки и стенки проксимального участка правой коронарной артерии (стрелка 4): a – до контраста; б – после введения омнискана
У пациентов контрольной группы отмечалось минимальное усиление интенсивности в стенке коронарных артерий, так что для ПКА ИУ составлял 1.08 ± 0,06, а для ЛКА 1,09 ± 0,07. При наличии же коронарного атеросклероза усиление было более значимым (рис. 1), индексы усиления представлены в таблице.
Показатели усиления интенсивности Т1-взв. спин-эхо изображений атеросклеротических бляшек и стенок артерий в зависимости от локализации. (достоверность различий p дана по сравнению с непораженными участками стенок артерий)
|
Инфаркт-связанная артерия |
Участки сосудистой стенки |
Индекс усиления интенсивности при контрастировании |
|
|
Левая коронарная артерия (огибающая ветвь) n = 12 |
Левая огибающая артерия |
Область бляшки |
1,54 ± 0,22 p < 0,05 |
|
Непораженный участок стенки |
1,22 ± 0,14 |
||
|
Правая коронарная артерия |
Область бляшки |
– |
|
|
Непораженный участок стенки |
1,18 ± 0,10 |
||
|
Правая коронарная артерия n = 10 |
Левая огибающая артерия |
Область бляшки |
– |
|
Непораженный участок стенки |
1,16 ± 0,12 |
||
|
Правая коронарная артерия |
Область бляшки |
1,42 ± 0,18 p < 0,05 |
|
|
Непораженный участок стенки |
1,20 ± 0,16 |
||
Как видно из представленных данных, вне зависимости от локализации коронарные бляшки достаточно интенсивно накапливали омнискан. Важно, что и в области непораженных участков артерий накопление контраста и усиление интенсивности происходило более выраженно, ‒ чем у лиц контрольной группы, показатели ИУ для которых приведены выше. Визуальная картина однозначно указывала на достоверное усиление в области стенки коронарных артерий, преимущественно в области атеросклеротических бляшек инфаркт-связанных артерий (рис. 1, 2).
Совершенствование технической базы МР-томографии привело сегодня к распространению высокопольных томографов с напряженностью поля от 1,5 Т до 3 Т [7]. Увеличение быстродействия при росте поля не отменяет того факта, что у лиц, требующих постоянного мониторирования состояния – а к их числу относятся все пациенты с неотложными кардиологическими и ангионеврологическими заболеваниями – закрытость магнита резко затрудняет контроль, повышает риск случайного развития осложнений в момент исследования. Кроме того, общепринято, что психологическая комфортность исследования на открытых системах намного выше, и это у пациентов с коронарным болевым синдромом также крайне важно. Учитывая, что современные открытые системы реализуют все кардиологические импульсные последовательности, что и высокопольные закрытые, за исключением спектроскопии, важность исследования коронарных бляшек при МРТ сердца на открытых системах не требует дальнейшего обоснования. Однако до сих пор такого исследования не было проведено, в первую очередь, вероятно, из-за недооценки возможностей современных открытых систем. Кроме того, в ряде случаев (наличие имплантатов, металлических протезов и пр.) исследование на высокопольных системах вообще противопоказано, в то время как на низкопольных аппаратах оно может быть проведено.
В представленном исследовании нам удалось показать, что подобно каротидным атеросклеротическим бляшкам [1] при коронарном атеросклерозе с перенесенным в бассейне соответствующей артерии инфарктом миокарда происходит достоверное контрастное усиление изображения, в первую очередь – атеросклеротической бляшки, но также и стенки сосуда в области нестенозированного участка. С одной стороны, накопление контраста было взаимосвязано с фактом повреждения в соответствующем артериальном бассейне (таблица, рис. 1, 2), а с другой – показатель ИУ оказался не коррелирующим ни со степенью коронарного стеноза, ни с тяжестью нарушения функции левого желудочка сердца. Такое положение, возможно, позволит в будущем полностью подтвердить на более широкой выборке, что интенсивное накопление парамагнетика в коронарной бляшке по сути означает независимый достоверный риск развития инфаркта и требует коррекции в виде стентирования или АКШ. По механизму контрастирования интенсивное накопление парамагнетика в бляшке означает формирование развитой сети vasa vasorum в ее толще. Между тем морфологически доказано, что формирование vasa vasorum достоверно связано с нестабильностью бляшки и повышенным риском повреждения [4].
Наши результаты показывают, что использование Т1-взвешенного режима спин-эхо в контрастированном исследовании миокарда для визуализации коронарных атеросклеротических бляшек вполне оправданно как дополнение и сочетание с протоколами inversion recovery, позволяющими выявить накопление парамагнетика в поврежденном миокарде [5]. В целом полученные здесь первые результаты парамагнитного контрастирования коронарных бляшек в Т1-взвешенном спин-эхо последовательности безусловно потребуют более широкого обобщения. В итоге это позволит обеспечить клинических кардиологов и кардиохирургов новой технологией неинвазивной визуализации коронарного атеросклероза и оценки его тяжести, тем более что открытые МРТ-сканеры в наилучшей степени пригодны для исследований у кардиологических пациентов.
Рецензенты:
Репин А.Н., д.м.н., профессор, зав. отделением реабилитации, главный кардиолог Областного отдела здравоохранения, г. Томск;
Буховец И.Л., д.м.н., старший научный сотрудник отделения рентгеновских и томографических методов диагностики, ФГБУ НИИ кардиологии СО РАМН, г.Томск.
Работа поступила в редакцию 04.02.2014.



