Рецидивирующее течение простого герпеса, особенно генитальной или аноректальной локализации, представляет серьезную как медицинскую, так и психосоциальную проблему, существенно ухудшая качество жизни пациента [1, 3, 4, 9, 11, 12]. Необходимо отметить возможную роль вируса простого герпеса 2-го типа (ВПГ-2) (во взаимодействии с хламидиями, микоплазмами, вирусами папилломы человека, цитомегаловирусом) в развитии онкологических заболеваний человека, в частности, рака предстательной железы и рака шейки матки. Предполагается, что ВПГ-2 может выступать как кофактор канцерогенеза, инициируя развитие дисплазии и поддерживая ее в состоянии стабилизации. Вирусы герпеса способны инициировать процессы атеросклероза, где ВПГ-2 выступает в ассоциации с цитомегаловирусом. Доказано неблагоприятное, часто фатальное влияние герпесвируса на течение беременности и родов, патологию плода и новорожденных. Описаны случаи диссеминации вируса с поражением последа и инфицированием плода [3].
Не менее важное значение имеет и тот факт, что активные проявления герпеса сопровождаются нарушением целостности защитного кожно-слизистого барьера, являются входными воротами для патогенных агентов, в том числе ВИЧ, а при наличии ВИЧ-позитивного статуса и вирусемии служат дополнительным фактором инфицирования лиц ближнего окружения [5, 6]. Установлено, что вирусы герпеса могут активировать геном вируса иммунодефицита человека, находящегося в стадии провируса, и являются кофактором прогрессирования ВИЧ-инфекции. Поэтому герпесвирусная инфекция является одной из СПИД-индикаторных инфекций [3, 4, 12].
При герпесвирусной инфекции поражаются эритроциты, тромбоциты, лейкоциты и макрофаги. Вирусы герпеса способны длительно персистировать в организме, формируя нестерильный иммунитет. При герпесе, как и при других хронических заболеваниях с персистенцией вируса, развиваются иммунодефицитные состояния, обусловленные недостаточностью различных звеньев иммунной системы и ее неспособностью элиминировать вирус из организма. Сохраняющиеся в течение всей жизни вируснейтрализующие антитела, хотя и препятствуют распространению, но не предупреждают развитие рецидивов [3, 4, 7, 12].
Трудно прогнозируемая частота рецидивирования герпеса, не всегда адекватный подход к назначению противовирусных средств из-за недопонимания их места в лечении герпесвирусной инфекции и, главное, нереалистические ожидания от терапии нередко обусловливают развитие пессимизма у врачей и психоэмоциональные нарушения у пациентов, вплоть до тяжелых депрессивных состояний и склонности к суициду [2, 7, 8, 10, 11].
Цель исследования – изучить наиболее часто встречающийся патологический микробиоценоз у пациентов с рецидивирующим генитальным герпесом и оценить его влияние на течение патологии.
Материал и методы исследования
Под наблюдением находились 105 пациентов (59 мужчин и 46 женщин в возрасте от 19 до 49 лет) с рецидивирующим течением генитального герпеса, в том числе с локализацией в области ягодиц – 10 случаев. Среди обследуемых лиц преобладали пациенты возрастной группы от 30 до 39 лет (таблица).
Возрастно-половой состав пациентов
|
Пациенты |
19–29 лет |
30–39 лет |
40–49 лет |
Всего |
|
Мужчины |
17 |
26 |
16 |
59 |
|
Женщины |
16 |
17 |
13 |
46 |
|
Всего |
33 |
43 |
29 |
105 |
При сборе анамнеза обращали внимание на частоту и тяжесть рецидивов, время последнего рецидива заболевания, сопутствующие болезни, в том числе инфекции, передающиеся половы путем (ИППП), проводимую терапию.
Клиническая картина складывалась из субъективных и объективных симптомов. К первым относили жалобы на болезненные высыпания в области половых органов и/или перианальной области; зуд, боль, парестезии в области поражения; болезненность во время половых контактов; зуд, жжение, болезненность при мочеиспускании (при локализации высыпаний в области уретры); слизисто-гнойные вагинальные выделения (при вагинальной локализации высыпаний); общие симптомы интоксикации (повышение температуры тела, головная боль, тошнота, недомогание, нарушения сна, боли в мышцах).
К объективным симптомам при манифестной форме генитального герпеса относили гиперемию и отечность кожных покровов и слизистых оболочек области поражения, единичные или множественные везикулезные элементы полициклической фестончатой формы на гиперемированном основании, локализующиеся в области поражения (после вскрытия которых оставались поверхностные, покрытые сероватым налетом эрозии размером 2–4 мм или сплошная эрозия с гладким дном и неподрытыми краями, окруженные ярко-красным ободком воспаления). Присоединение вторичной инфекции сопровождалось появлением гнойного экссудата, отмечалось увеличение и болезненность паховых лимфатических узлов.
Атипичные формы генитального герпеса характеризовались гиперемией и отечностью области поражения при отсутствии патологических высыпаний или появлением рецидивирующих трещин слизистой оболочки наружных половых органов, которые самостоятельно эпителизировались в течение нескольких дней. Наблюдались везикулезные элементы с геморрагическим содержимым (геморрагическая форма), зудящие пятна или папулы, разрешающиеся за 1–3 дня (абортивная форма), кратковременное появление на слизистой оболочке наружных половых органов поверхностных трещинок, сопровождающихся незначительным зудом (субклиническая форма).
Всем пациентам наряду с общеклиническими, общехимическими и инструментальными обследованиями проводили исследования на выявление сифилиса, вируса иммунодефицита человека, гепатиты В и С, урогенитальные инфекции (гонорею, трихомониаз, хламидиоз, микоплазмозы). Применяли бактериоскопические, бактериологические, молекулярно-биологические методы и иммуноферментный анализ с использованием соответствующих тест-систем по стандартным методикам. Иммунологическими методами определяли наличие антител (IgM, IgG) к простому герпесу типа 1 и 2. Для идентификации вирусов 1 и 2-го типов из очагов поражения использовали молекулярно-биологический метод. Всех больных тщательно осматривали на наличие дерматозов, обусловленных папилломавирусной инфекцией: остроконечные кондиломы, бородавки (плоские, обыкновенные), папилломы, а также на контагиозный моллюск.
В зависимости от полученных результатов пациентам наряду с противовирусным лечением назначали соответствующую терапию. Оценивали ближайшие результаты лечения (контроль излеченности сопутствующих ИППП, динамику регресса симптомокомплекса рецидива герпесвирусной инфекции) и отдаленные результаты (частоту рецидивов, степень их выраженности).
Результаты исследования и их обсуждение
При оценке особенностей течения дерматоза установлено, что тяжелое течение герпеса (более 6 рецидивов в год) было у 49 (46,7 %) больных, в том числе у 9 женщин в течение последнего года были ежемесячные обострения, связанные с началом менструального цикла. У 19 больных наблюдалось 9–10 рецидивов в течение последних 2 лет, у 26 больных – 7–8 рецидивов в год. У 35 (33,3 %) человек имело место среднетяжелое течение патологии (4–6 рецидивов в год), у 21 (20 %) больного – легкое течение с развитием не более 3 рецидивов в год в течение последних 2 лет (рис. 1).
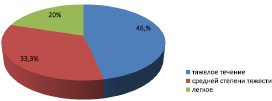
Рис. 1. Распределение пациентов с рецидивирующим герпесом по тяжести течения
Жалобы на болезненные высыпания в области половых органов предъявляли 27 (25,7 %) человек, в перианальной области ‒ 10 (9,5 %). Зуд, боль, парестезии в области поражения беспокоили 29 (27,6 %) пациентов. Болезненность во время половых контактов отмечали 12 (11,4 %) человек, зуд, жжение, болезненность при мочеиспускании – 17 (16,2 %) пациентов. На слизисто-гнойные вагинальные выделения жаловались три женщины. Общие симптомы интоксикации наблюдались у 16 (15,2 %) больных.
Манифестная форма генитального герпеса наблюдалась у 48 (45,7 %) пациентов, из них присоединение вторичной инфекции во время последнего рецидива отмечено у 4 (3,8 %), увеличение и болезненность паховых лимфатических узлов у 25 (23,8 %) человек.
Атипичные формы генитального герпеса обнаружены у 57 (54,3 %) пациентов, из них с гиперемией и отечностью области поражения при отсутствии патологических высыпаний – 24 (22,9 %), появлением рецидивирующих трещин слизистой оболочки наружных половых органов – 16 (15,2 %), образованием везикулезных элементов с геморрагическим содержимым – 2 (1,9 %), зудящими пятнами – 11 (10,5 %), кратковременным появлением на слизистой оболочке наружных половых органов поверхностных трещинок, сопровождающихся незначительным зудом – 4 (3,8 %) человека.
По результатам комплексного клинико-лабораторного и инструментального обследований, у 99 (94,3 %) больных выявлены сопутствующие урогенитальные инфекции. Так, у 24 (24,2 %) пациентов был диагностирован урогенитальный трихомониаз, у 10 (10,1 %) больных – смешанная трихомонадно-хламидийная инфекция, у 17 (17,2 %) – трихомонадно-микоплазменная, у 13 (13,1 %) – трихомонадно-уреоплазменная, у 11 (11,1 %) – трихомонадно-кандидозная, у 12 (12,1 %) – хламидийно-микоплазменная, у 5 (5,1 %) – хламидийная, у 7 (7,1 %) – хламидийно-кандидозная инфекция (рис. 2).
Гепатит С выявлен у 8 (8,1 %) человек, гепатиты В и С – у 2 (2 %) пациентов.
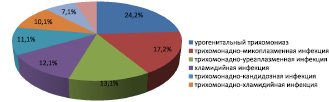
Рис. 2. Характеристика патологического микробиоценоза у пациентов с рецидивирующим генитальным герпесом
У каждого из 105 обследованных больных обнаружены бактериальные и/или вирусные инфекции, протекавшие торпидно или бессимптомно, но требовавшие соответствующей лечебной коррекции. Наряду с лечением дерматоза всем пациентам проведена терапия сопутствующей половой инфекции. Переносимость лечения у всех больных была удовлетворительной. Мониторинг общеклинических и биохимических анализов, проводимых в процессе лечения, не выявил каких-либо изменений, требующих отмены препарата. Проведенный контроль излеченности ИППП показал, что у 78 (85,7 %) пациентов была достигнута эрадикация возбудителей.
При анализе отдаленных (около 2 лет) результатов лечения снижение частоты рецидивов заболевания отмечено в 64 (61 %) случаях. У 63,3 % пациентов с тяжелым и у 57,1 % со среднетяжелым течением герпеса число рецидивов уменьшилось до 1–3 раз в год, у 14,3 и 17,1 % сократилось до 3–4 рецидивов в год соответственно. У 26 (24,8 %) больных рецидивов не отмечено вовсе (рис. 3). В 15 (14,2 %) наблюдениях частота рецидивов после окончания терапии сочетанной инфекции существенно не изменилась, совпадая с неудовлетворительными результатами лечения сопутствующих ИППП.
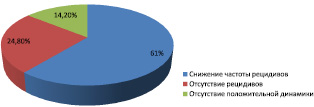
Рис. 3. Отдаленные результаты комплексного лечениярецидивирующего генитального герпеса и ИППП
Заключение
Клинико-лабораторное и инструментальное обследование 105 пациентов с рецидивирующим течением простого герпеса выявило у 99 (94,3 %) из них сопутствующие урогенитальные инфекции, протекавшие торпидно или бессимптомно, но требовавшие проведения соответствующей лечебной коррекции. В 75,2 % случаев встречался урогенитальный трихомониаз. При анализе отдаленных (около 2 лет) результатов лечения сочетанной патологии отмечено снижение частоты рецидивов у 61 % больных, у 24,8 % в течение 2 лет рецидивов не отмечено вовсе. В 14,2 % наблюдений частота рецидивов после окончания терапии сочетанной инфекции существенно не изменилась, совпадая с неудовлетворительными результатами лечения сопутствующих ИППП. Таким образом, комплексный подход к обследованию и лечению пациентов с рецидивирующим генитальным герпесом позволил уменьшить количество рецидивов дерматоза.
Рецензенты:
Горчаков В.Н., д.м.н., профессор, заведующий лабораторией функциональной морфологии, ФГБУ «Научно-исследовательский институт клинической и экспериментальной лимфологии» Сибирского отделения СО РАМН, г. Новосибирск;
Селятицкая В.Г., д.б.н., профессор, заведующая лабораторией эндокринологии и заместитель директора по научной работе, ФГБУ «Научный центр клинической и экспериментальной медицины» Сибирского отделения РАМН, г. Новосибирск.
Работа поступила в редакцию 04.07.2013.



