Управление солюбилизационными характеристиками лекарственных веществ является одним из основных направлений в разработках современных систем доставки лекарств (Drug Delivery Systems) [22]. В этом направлении наиболее востребованы методы повышения растворимости и скорости растворения активных фармацевтических субстанций – лекарственных веществ (ЛВ). Растворимость играет существенную роль в действии лекарств, прежде всего предназначенных для перорального приема, так как максимальная скорость пассивного транспорта препарата через биологические мембраны – основной путь для поглощения ЛВ – зависит от проницаемости мембраны и концентрации раствора/растворимости. Учитывая, что ~40 % выпускающихся лекарственных субстанций классифицируются как практически нерастворимые, а ~85 % самых продаваемых препаратов в США и Европе принимаются перорально, актуальность исследований в данном направлении становится очевидной.
В настоящее время FDA принята система биофармацевтической классификации лекарств [24, 26] для прогнозирования биодоступности при пероральном приеме. Эта система основана на использовании соотношений параметров растворимости и проницаемости стенок желудочно-кишечного тракта (ЖКТ). Растворимость классифицирована на основании стандартов Фармакопеи США (USP) [23]. Так, лекарственное вещество считается хорошо растворимым, когда максимальная разрешенная его доза растворяется в < 250 мл воды в диапазоне рН от 1,0 до 7,5. Классификация биодоступности из ЖКТ основана на сравнении с внутривенной инъекцией. Считается, что лекарственное вещество обладает высокой биодоступностью, если ~ > 90 процентов его дозы проникает в кровоток при пероральном введении. Ниже приводятся основные классы ЛВ по критериям «проницаемость стенок ЖКТ – растворимость».
Класс I – высокая проницаемость, высокая растворимость. Эти соединения хорошо всасываются и скорость абсорбции, как правило, выше, чем выведение.
Класс II – высокая проницаемость, низкая растворимость. Пример: большинство нестероидных противовоспалительных средств. Биодоступность таких продуктов ограничена скоростью их растворения (кинетический барьер) и растворимостью (термодинамический барьер). К этому классу относится ~> 30 % выпускающихся и разрабатываемых лекарств.
Класс III – низкая проницаемость, высокая растворимость. Пример: большинство антибиотиков бета-лактамного типа. Низкая скорость абсорбции ограничивает проникновение в кровоток, но препараты растворяются очень быстро.
Класс IV – низкая проницаемость, низкая растворимость. Пример: антигельминтики – альбендазол, карбендацим, фенбендазол; растительные флавоноиды – рутин, кверцетин, дигидрокверцетин. Эти соединения имеют низкую биодоступность. Обычно они плохо поглощаются слизистой оболочкой кишечника. К этому классу относится ~ 10 % выпускающихся и разрабатываемых лекарств.
Таким образом, ЛВ, относящиеся к II и IV классам, нуждаются в технологиях повышения их водорастворимости. К этим классам относятся до 50 % разрабатываемых и выпускающихся фармацевтической промышленностью ЛВ.
Для повышения растворимости лекарств используют различные физико-химические подходы: уменьшение размеров частиц, модификация кристаллической структуры, получение твердых дисперсий ЛВ с наполнителями и т.д. [20, 18]. Так, при измельчении субстанций антигельминтных препаратов «карбендацим» (бензимидазолил-2-метил карбамат) и «альбендазол» (5-тиопропилбензимидазолил-2-метилкарбамат) в планетарно-центробежном активаторе АГО–2 в «жестких» условиях активации (40 – 60g) было показано не только уменьшение размера частиц, но также стабильность химической структуры, а именно, при сравнении ИК-спектров исходных и измельченных субстанций не было обнаружено изменений в расположении полос поглощения основных функциональных групп (NH, C = N, C = O, OCH3). В спектрах измельченных субстанций наблюдалось увеличение интенсивности этих сигналов, что позволило предполагать лишь о разрушении межмолекулярных водородных связей [11]. Изучение растворения исходного и измельченного образцов карбендацима в среде «желудочного сока» показало, что скорость растворения измельченной субстанции выше, нежели неизмельченной субстанции.
Однако, по нашему мнению, наиболее значимые результаты достигаются за счет перевода ЛВ в их водорастворимые соли (если ЛВ имеет выраженные кислотно-основные свойства), а также за счет включения молекул ЛВ в супрамолекулярные водорастворимые образования (межмолекулярные комплексы, мицеллы) со специально подобранными «вспомогательными» веществами.
Механохимия является разделом химии твердого тела, в котором изучаются физико-химические превращения твердых веществ и их смесей в условиях интенсивных ударно-истирающих воздействий, обычно реализующихся в специальных мельницах. На рис. 1 показаны возможные пути трансформаций в смесях твердых веществ при их механохимической обработке [3].
Суть нашей технологии заключается в получении твердых дисперсий лекарственных веществ со вспомогательными веществами различной химической природы. Увеличение растворимости ЛВ и повышение эффективности фармакологического действия в зависимости от их физико-химических свойств достигается:
– образованием твердых дисперсий, в которых ЛВ диспергировано в молекулярной форме или находится в аморфном состоянии;
– образованием водорастворимых солей;
– образованием водорастворимых комплексов включения с полисахаридами по типу «гость-хозяин», а также мицелл.
Далее мы рассмотрим вышеуказанные случаи.
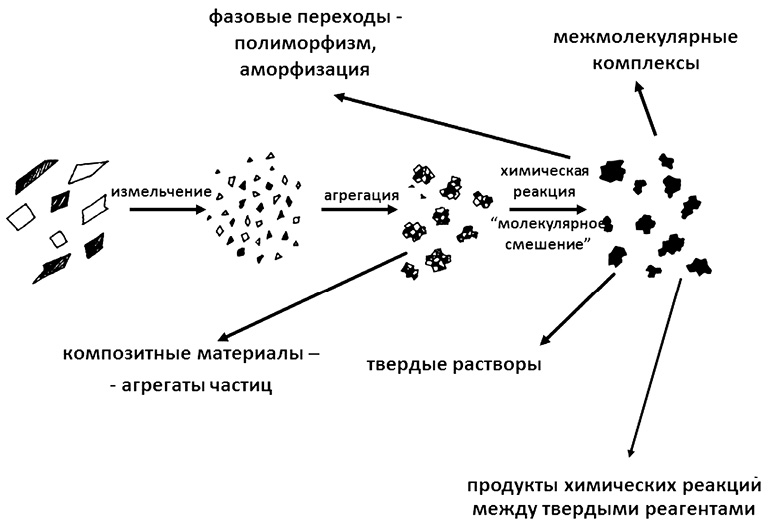
Рис. 1. Схема механохимических превращений в смесях твердых веществ (ЛВ + вспомогательные вещества) при их механической обработке ударно-истирающими воздействиями
Получение и свойства твердых дисперсий, в которых ЛВ находится в аморфизованном состоянии или диспергирована в молекулярной форме
Высвобождение в раствор фармакологически активного вещества из твердых лекарственных форм (порошков, таблеток и т.д.) во многом определяется скоростью растворения его кристаллической фазы. Однако многие фармакологические активные вещества крайне медленно растворяются в воде во многом за счет плохой смачиваемости и «прочности» кристаллической решетки. Очевидно, что получение твердых растворов – молекулярных дисперсий – таких веществ в хорошо растворимом наполнителе либо разупорядочение их кристаллических фаз будет способствовать ускорению процесса растворения. Именно этот принцип был применен нами к модификации антигельминтика карбендацима и ряда транквилизаторов бензодиазепинов – диазепама, оксазепама и медазепама, лекарственные субстанции которых практически нерастворимы в воде.
Для модификации солюбилизационных характеристик бензодиазепинов нами механохимическим способом были получены их твердые дисперсии с лактозой и микрокристаллической целлюлозой в весовых соотношениях 1:5, 1:10 и 1:15. В дифрактограммах механически активированных образцов наблюдалось резкое падение интенсивности рефлексов (без их заметного уширения) кристаллических фаз ЛВ вплоть до их полного исчезновения. Рефлексы веществ – наполнителей (лактозы и отчасти целлюлозы) претерпевали уширение, что свидетельствовало о накоплении дефектов и уменьшении кристалличности. К сожалению, методы термического анализа оказались неэффективны из-за относительно низких температур разложения веществ-наполнителей.
Проведенные исследования растворимости образцов продемонстрировали во всех случаях увеличение скорости растворения ЛВ в механохимически полученных образцах по сравнению со смесями, не подвергавшимися механохимической обработке и тем более измельченными исходными субстанциями [5]. Проведенные испытания биологической доступности образцов модифицированных препаратов оксазепама на лабораторных животных – кроликах – показали увеличение действующей концентрации оксазепама в крови и сокращение времени достижения ее максимального значения. Биодоступность оксазепама по сравнению с неактивированной смесью увеличивается в 1,56 ± 0,25 раза. Таким образом повышается эффективность действия лекарственного средства.
Получение и свойства твердых дисперсий, образующих водорастворимые соли ЛВ
Многие малорастворимые ЛВ обладают кислотными или основными свойствами и способны к ионизации в водных растворах и образованию соответствующих солей. Как правило, ионизированная форма является более гидрофильной и имеет более высокую водорастворимость. Многие ЛВ с целью повышения их растворимости выпускаются в виде их солей [9, 12]. Так, лекарственные вещества, имеющие основной характер, – в виде гидрохлоридов, а органические кислоты – в виде солей металлов или органических оснований. Соли получают реакцией жидкофазной нейтрализации с последующим выделением (сушкой). При этом требуются большие объемы растворителей, громоздкое оборудование, значительные производственные площади. Кроме того, в процессе сушки возможно разложение целевого продукта.
Рассмотрим возможности этого подхода на примере ацетилсалициловой кислоты (аспирина). Малая растворимость в воде (< 0,25 % при комнатной температуре) снижает ее фармакологическую эффективность и вызывает нежелательные побочные эффекты при использовании ее в составе лекарственных средств. Соли ацетилсалициловой кислоты с щелочными и щелочноземельными металлами были синтезированы еще в начале ХХ века и обладают повышенной в ~102 раз растворимостью. Фармакологические испытания показали их явные преимущества по сравнению с исходной ацетилсалициловой кислотой. Повышение растворимости и скорости растворения ацетилсалицилатов способствует более быстрому достижению максимальной концентрации в крови, то есть ускоряет действие лекарства. В свою очередь более высокая действующая концентрация способствует увеличению фармакологического эффекта и отмечается снижение нежелательного эффекта – раздражение желудка (ульцерогенный эффект) [16, 10].
Однако при очевидных преимуществах использования солей АСК в качестве лекарственного средства эти препараты выпускаются в малых объемах и отличаются высокой ценой. Дело в том, что все существующие технологические процессы получения солей проводятся в водной или в водно-спиртовой фазах с последующей сушкой продукта. При этом ацетилсалициловая кислота частично претерпевает разложение на салициловую и уксусную кислоты за счет гидролиза в водных растворах [19]. Существующие требования к чистоте продукта значительно усложняют технологию производства ацетилсалицилатов и ведут к удорожанию продукции.
Альтернативным путем являются так называемые «шипучие» (effervescent) или «буферированные» (buffered) лекарственные средства (например, [17]), с физико-химической точки зрения представляющие из себя твердые дисперсные системы, содержащие субстанцию АСК и щелочные агенты – карбонаты металлов. При этом для ускоренного разрушения таблетки (гранулы) в эту массу добавляются водорастворимые фармакологически допустимые органические кислоты, которые при гидратации ускоренно реагируют с карбонатами металлов, выделяя углекислый газ. Эффект солеобразования достигается при растворении таких таблеток или гранул. При таком подходе в композицию добавляется значительный избыток нейтрализующих веществ по сравнению с количеством, необходимым для нейтрализации только ацетилсалициловой кислоты. В качестве примера можно привести патент [15], где предлагается следующее соотношение компонентов: лекарственное вещество (ацетилсалициловая кислота, ацетаминофен или кетопрофен) – 0,2–16 вес. %, лимонная кислота – 26–40 вес. %, нейтрализующие агенты (смесь NaHCO3, КНСО3, СаСО3) – 28–47 вес. %. Технология их производства, как правило, включает стадии влажного гранулирования по отдельности щелочных и кислотных компонентов, затем смешение полученных гранул и таблетирование. Характерным недостатком описываемых препаратов является низкое весовое содержание ацетилсалициловой кислоты – в приведенных примерах 10–16 %, а общий вес единичной дозы достигает 2,5–3,5 г. Такие таблетки невозможно глотать, их можно принимать только после растворения в довольно большом объеме воды. Кроме того, вспомогательные вещества по некоторым показателям (например, содержание натрия) нежелательны для приема пациентами. Увеличенная материалоемкость повышает себестоимость лекарственных средств.
Вследствие описанных недостатков промышленно выпускаемых солевых лекарственных форм ацетилсалициловой кислоты в мире известны единицы, а в нашей стране их просто нет. Основываясь на имеющемся у нас опыте, мы применили механохимический подход для получения растворимых форм ацетилсалициловой кислоты с целью последующего использования их в качестве лекарственных средств. Ранее нами [13] было установлено, что ацетилсалициловая кислота вступает в механохимическую реакцию нейтрализации с карбонатами и бикарбонатами щелочных металлов – натрия и калия – с образованием их солей. Эта реакция проходит полностью за несколько минут при обработке реагентов в энергонапряженных планетарных мельницах. Однако химический анализ с помощью ВЭЖХ показывает образование значительного количества примеси салициловой кислоты (в виде ее салицилатов) от 7 до 30 % от ацетилсалициловой. «Начальное» содержание салициловой кислоты (СК) не превышает 0,1 %. Причиной же значительного (до 30 %) увеличения СК, очевидно, является реакция гидролиза с образующейся в результате нейтрализации водой. Согласно принятым фармакопейным нормам [25], относительное содержание СК в растворимых лекарственных средствах на основе АСК не должно превышать 3–8 %. Таким образом, подход прямой механохимической нейтрализации для получения растворимых препаратов ацетилсалициловой кислоты неприемлем по причине ее химической нестабильности в условиях механохимической реакции и хранения. Отметим, что этот подход может оказаться продуктивным в случае химических веществ, обладающих большей стабильностью.
При исследовании вышеуказанных механохимических процессов мы обнаружили явление образования композитных агрегатов частиц твердых реагентов как промежуточной стадии механохимической реакции [14, 4], что было показано на рис. 1. Эти материалы, представляющие собой композитные материалы – твердые дисперсные системы веществ-реагентов, обладают повышенной реакционной способностью. Они представляют собой подготовленную к химическому взаимодействию систему, причем это взаимодействие легко может быть запущено и проведено до конца относительно слабыми (не механическими) воздействиями – гидратацией или нагревом. Таким образом, в определенной ситуации возможно использование механохимически полученных композитов вместо конечных продуктов химического взаимодействия. В этом случае условия механической обработки могут быть значительно мягче. Возможно использование малоэнергонапряженных мельниц-активаторов, а в приложении к проточным виброцентробежным мельницам можно ожидать достаточно высокой производительности по выходу обработанного материала. На основе этого подхода мы разработали метод получения быстрорастворимых порошков ряда лекарственных средств – нестероидных противовоспалительных препаратов, в частности, на основе ацетилсалициловой кислоты. В качестве нейтрализующих веществ мы использовали безводные карбонаты металлов – лития, натрия, калия, кальция и магния. Стехиометрическое соотношение выбиралось с расчетом получения кислой соли в случае щелочных металлов для уменьшения вероятности образования свободной воды. Для щелочноземельных металлов соотношение компонентов обеспечивало полную реакцию нейтрализации при гидратации образца с образованием прозрачных растворов.
Сопоставление данных ИК-спектроскопии и рентгеноструктурного анализа позволили сделать вывод, что даже при длительной механической обработке смесей относительно слабыми механическими воздействиями в валковых ротационных мельницах в течение нескольких часов не наблюдается заметной реакции нейтрализации. Электронные микрофотографии исходных веществ и дисперсий приведены на рис. 2.
При растворении смесей, не подвергавшихся механической обработке, их компоненты растворяются с различной скоростью. В первую очередь растворяются карбонаты щелочных металлов, а затем в уже образовавшемся щелочном растворе растворяется ацетилсалициловая кислота. Общее время растворения составляет несколько минут и зависит от скорости перемешивания. При использовании малорастворимых карбонатов щелочноземельных металлов время растворения может достигать нескольких часов. В противоположность этому полученные механохимическим путем композитные порошки очень быстро (за несколько секунд) полностью растворяются в воде с легким газовыделением, а растворение карбонатов и АСК проходит одновременно. Этот способ получения быстрорастворимых дисперсных систем является оригинальным [7, 8].
Реализация условий, описанных в патентах, и проведение комплексных первичных оценок химической стабильности ацетилсалициловой кислоты при получении и хранении быстрорастворимых порошков, изучении скоростей их растворения и условий получения позволили выявить оптимальные составы (АСК/Na2CO3 = 64/36 вес. % и АСК/CaCO3 = 78/22 вес. %), которые были использованы для дальнейшей разработки лекарственных средств. При этом общее количество вспомогательных веществ составляло 36–22 вес. %, что значительно меньше, чем в известных быстрорастворимых формах аспирина, и это рассматривается как один из основных их недостатков. При терапевтической дозировке в 0,325–0,500 г АСК наши таблетки по весу вполне пригодны для приема путем проглатывания. Учитывая, что скорость всасывания АСК в желудке составляет ~0,25 1/ч, желательно добиться, чтобы время полного растворения таблетки в желудке не превышало 15 мин. В этом случае способ проглатывания таблетки будет фармакологически эквивалентен приему раствора. Вместе с тем необходимо оставить возможность приема препарата в виде раствора после предварительного растворения таблетки, то есть максимально ускорить растворение таблетки. Эти два требования сочетаются при времени растворения 2–10 мин. Наибольшее влияние на скорость растворения таблеток, полученных из порошкообразных твердых дисперсных систем АСК/карбонаты металлов, оказывает фактор давления прессования. Эксперименты показали, что эта величина должна быть в пределах 3,0–7,5∙107 н/м2. При меньшем давлении прессования таблетки не обладают необходимой прочностью, а при увеличенном – слишком медленно растворяются.
а)  б)
б)  в)
в) 
Рис. 2. Электронные микрофотографии: а – карбонат натрия; б – ацетилсалициловая кислота; в – дисперсия/агрегат частиц состава АСК/Na2CO3 64/36 по весу (эквимолярное соотношение), полученная при механической обработке исходных компонентов в шаровой мельнице с энергонапряженностью 1g. Масштаб указан на микрофотографиях
В табл. 1 приведены фармакокинетические характеристики разработанных нами растворимых таблеток состава АСК/Na2CO3 = 64/36 вес. % и препарата – аналога «Аспирин + С» (Байер, Германия), полученные при испытаниях на лабораторных животных – кроликах − в ВНИИ фармакологии МЗ РФ, подтверждающие биоэквивалентность препаратов и способов приема. На рис. 3 показана динамика изменения концентрации салициловой кислоты (метаболита АСК) в крови лабораторных животных (кроликов) после перорального приема раствора таблеток «Аспирин + С» (1), раствора таблеток нашего препарата (2) и таблеток нашего препарата без предварительного растворения (3) в эквивалентных по АСК дозах.
Таблица 1
Фармакокинетические характеристики препаратов ацетилсалициловой кислоты
|
Препарат, способ приема * |
Сmax, мкг/мл |
Tmax, ч |
AUC |
Скорость всасывания, ч–1 |
|
Аспирин + С, БАЙЕР, ФРГ, раствор |
397,0 ± 25 |
0,58 ± 0,08 |
1714,7 ± 258 |
0,25 ± 0,04 |
|
АСК / Na2CO3, раствор |
429,5 ± 31 |
0,5 ± 0,1 |
1869,5 ± 267 |
0,26 ± 0,031 |
|
АСК / Na2CO3, таблетки |
417,5 ± 29 |
0,7 ± 0,1 |
1852,8 ± 268 |
0,25 ± 0,03 |
Примечания:
Cmax – максимальная концентрация в крови;
Tmax – время достижения максимальной концентрации в крови;
AUC – площадь под фармакокинетической кривой, в относительных единицах;
* – навески препаратов взяты в эквивалентных по действующему веществу концентрациях.
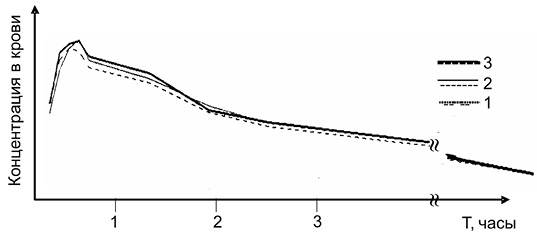
Рис. 3. Фармакокинетика препаратов «АСК – Na2CO3» и «Аспирин + С» при разных способах приема препаратов. Прием раствора таблеток «Аспирин + С» (1), раствора таблеток нашего препарата (2) и таблеток нашего препарата без предварительного растворения (3) в эквивалентных по АСК дозах
В соответствии с действующими правилами нами были разработаны фармакопейные статьи на таблетки и субстанцию, проведены фармакологические испытания [1, 2] и препарат зарегистрирован для применения в РФ.
Композиция состава АСК/CaCO3 = 78/22 вес. % также представляет значительный интерес. Она обладает высокой химической стабильностью при хранении и меньшей гигроскопичностью, но замедленной скоростью растворения. Методом прямого прессования из нее были получены таблетки с двумя дозировками АСК – 0,1 г (вес таблетки 0,128 г) и 0,5 г (вес таблетки 0,64 г). По своим характеристикам – химическая чистота, время растворения, кислотонейтрализующая емкость (для таблеток по 0,5 г) – эти таблетки соответствуют требованиям USP к так называемым «буферированным» таблеткам ацетилсалициловой кислоты. Разработанный нами препарат, получивший название «Антиагрегин», показал при сравнительных опытах с применяемыми в медицинской практике импортными препаратами практически равнозначную эффективность и безопасность для лечения и профилактики сердечно-сосудистых заболеваний (табл. 2).
Таблица 2
Сравнительные характеристики разработанных в ИХТТМ СО РАН растворимых таблеток и их импортных аналогов
|
Характеристики таблеток |
АСК – CaCO3 |
АСК – Na2CO3 |
Аспирин + C BAYER |
Упсарин UPSA |
|
Диаметр таблетки, мм |
12 |
12 |
27 |
23 |
|
Высота таблетки, мм |
4,7 |
4,7 |
4,0 |
5,5 |
|
Вес таблетки, грамм |
0,64 |
0,64 |
3,3 |
3,5 |
|
Содержание АСК, грамм |
0,50 |
0,40 |
0,40 |
0,33 |
|
Относительное содержание АСК, % |
78,5 |
64,0 |
12,1 |
9,4 |
|
Время полного растворения в 100 мл воды, минут: |
||||
|
При температуре + 25 °C |
10–20 |
4–6 |
2–3 |
1–2 |
|
При температуре + 35 °C |
5–10 |
1–3 |
1 |
0,5–1 |
|
Объем CO2, выделяющийся при растворении, мл |
||||
|
– в воде |
20 |
6,5 |
75 |
100 |
|
– в 0,1 н HCl |
31 |
25 |
< 200 |
< 200 |
Учитывая высокую химическую стабильность дисперсии АСК/СаСО3 с их относительным содержанием 78,2/21,8 вес. %, могут быть разработаны несколько разновидностей растворимых таблеток, отличающихся не только общим весом и дозировкой ацетилсалициловой кислоты, но и добавками других фармацевтических субстанций, например, витамина С, парацетамола и т.д.
Анализ данных табл. 2 позволяет убедиться в следующих преимуществах разработанных нами таблеток:
– общий вес таблетки уменьшен в 5 раз;
– уменьшено количество вспомогательных веществ;
– значительно снижено газовыделение при растворении;
– свойственная лишь нашим таблеткам возможность приема препарата как путем проглатывания таблетки, запивая водой, так и после его предварительного растворения. Для импортных аналогов проглатывание таблетки невозможно из-за ее величины и большого газовыделения;
– уменьшение себестоимости производства в 3–4 раза.
Обнаруженный эффект образования агрегатов реагентов при механическом воздействии носит общий характер и свойственен большому числу органических веществ. Еще одним примером использования этого явления для повышения растворимости растительных флавоноидов является механохимическое получение их твердых дисперсий с карбонатами кальция и магния. Растительные флавоноиды (ФЛ) являются полифенольными соединениями, обладающими кислотными свойствами. Однако эти вещества, как правило, не образуют солей с ионами металлов, следовательно, невозможно их выделение и использование в виде индивидуальных ЛВ. Тем не менее, в щелочных диапазонах рН, их молекулы способны к ионизации, и доля ионизованной формы определяется величиной рН и рКа.
ФЛ–ОН + ОН– ↔ ФЛ–О– + Н2О
Как правило, ионизованная форма имеет более высокую водорастворимость. Таким образом, смещая равновесие в сторону ионизованных молекул, мы повышаем общую концентрацию (растворимость определяется как сумма ионизированных и нейтральных молекул) флавоноидов в растворе. В качестве щелочных агентов, позволяющих «смещать» рН в необходимый слабощелочной диапазон, мы использовали «фармакопейные» субстанции карбонатов кальция и магния. Результаты исследования растворимости флавоноидов (на примере рутина и дигидрокверцетина) из их механохимически полученных твердых дисперсий с карбонатами приведены в табл. 3.
Таблица 3
Показатели растворимости флавоноидов рутина и дигидрокверцетина (ДГК) из их механохимически полученных твердых дисперсий с карбонатами кальция и магния
|
Вещество/композиция (массовое отношение) |
Растворимость вещества/композиции, г/л |
Увеличение растворимости в n раз |
рН |
|
Рутин |
0,065 |
|
|
|
Рутин + MgCO3 (осн) (3:1) |
2,2 |
33,8 |
8,426 |
|
Рутин + MgCO3 (осн) (1:5) |
2,96 |
45,5 |
8,543 |
|
Рутин + MgCO3 (осн) (1:10) |
2,63 |
40,5 |
8,637 |
|
Рутин + СаCO3 (3:2) |
0,61 |
9,4 |
8,018 |
|
Рутин + СаCO3 (1:5) |
1,3 |
20 |
8,392 |
|
Рутин + СаCO3 (1:10) |
1,02 |
15,7 |
8,476 |
|
Рутин + АГ (1:10) |
0,07 |
1,1 |
3,431 |
|
Рутин + АГ (1:20) |
0,09 |
1,4 |
3,491 |
|
Дигидрокверцетин (ДГК) |
1,079 |
|
|
|
ДГК + MgCO3 (осн) (2:1) |
23,8 |
22,1 |
7,544 |
|
ДГК + MgCO3 (осн) (1:1) |
20,7 |
19,2 |
7,635 |
|
ДГК + MgCO3 (осн) (1:2) |
16,68 |
15,5 |
7,586 |
|
ДГК + СаCO3 (1:2) |
6,95 |
6,4 |
7,26 |
|
ДГК + СаCO3 (2:1) |
4,79 |
4,4 |
7,121 |
|
ДГК + СаCO3 (1:1) |
5,66 |
5,3 |
7,05 |
Также на примере флавоноидов кверцетина и дигидрокверцетина нами показано, что повышение растворимости имеет следствием усиление антиоксидантной активности, а также капилляропротективного действия [21, 6].
В заключение подчеркнем, что получение твердых дисперсий веществ – реагентов, которыми являются кислоты и основания, невозможно с помощью традиционных технологий, использующих жидкие фазы или расплавы, и может быть осуществлено только с помощью твердофазной механохимической технологии.
Заключение
Рассмотрена важность вопроса повышения водорастворимости малорастворимых лекарственных веществ с целью создания высокоэффективных лекарственных средств. Обоснована эффективность механохимической технологии для получения твердых дисперсий лекарственных веществ с вспомогательными веществами с целью повышения их водорастворимости.
Описано получение и свойства твердых дисперсий, в которых лекарственные вещества находятся в аморфизованном состоянии. Рассмотрены получение и свойства твердых дисперсий ЛВ кислотного характера и вспомогательных веществ щелочной природы, образующих при гидратации водорастворимые соли ЛВ. В последнем случае достигаются наиболее высокие показатели водорастворимости. Это продемонстрировано на примерах ЛВ – ацетилсалициловой кислоты и растительных флавоноидов. На основании механохимической технологии получения твердых дисперсий разработано и зарегистрировано в РФ лекарственное средство быстрорастворимой ацетилсалициловой кислоты.
Рецензенты:
Мордвинов В.А., д.б.н., заведующий лабораторией молекулярной и клеточной биологии, заместитель директора по научной работе Института цитологии и генетики СО РАН, г. Новосибирск;
Верещагин Е.И., д.м.н., профессор, заведующий кафедрой анестезиологии и реаниматологии Новосибирского государственного медицинского университета, г. Новосибирск.
Работа поступила в редакцию 29.11.2012.



