В настоящее время кератопластика у ряда больных с развитой стадией эндотелиально-эпителиальной дистрофии является единственной возможностью купирования патологического процесса, зрительной реабилитации. Последние 30-40 лет для лечения таких дистрофий использовалась сквозная кератопластика, техника которой хорошо отработана и существенно не менялась. Известно, что при сквозной кератопластике риск развития реакции тканевой несовместимости выше, чем при послойной. Однако оптические результаты традиционной послойной пересадки роговицы, как правило, уступают результатам сквозной кератопластики. Это связано с возможностью развития более выраженного неправильного послеоперационного астигматизма и избыточного светорассеяния на границе трансплантата и ложа реципиента в результате рубцевания в этой зоне.Эндотелиальная (задняя послойная) кератопластика заключается в замещении вовлеченных в патологический процесс задних слоев роговицы и эндотелия при сохранении собственных передних слоев [2, 4, 8, 9]. Предложенная в 70-х годах мануальная задняя послойная кератопластика [5, 10] не нашла широкого применения из-за сложности выполнения и осложнений, характерных для послойных кератопластик.
В последние годы исследования направлены на разработку, усовершенствование и оптимизацию способов и техники послойной кератопластики на основе современных технологий [2, 3, 7]. Современный комплекс диагностического оборудования дает новые возможности оценки результатов хирургического лечения роговицы, как в функциональном плане, так и по гистологическим и биомеханическим критериям. В 1996 году Busin на конгрессе Американской Офтальмологической Академии доложил об одном из современных вариантов эндотелиальной кератопластики с формированием лоскута собственных передних слоев при применении микрокератома. Данное исследование посвящено клиническому изучению аналогичной техники оперативного вмешательства [6].
Целью работы является комплексная оценка результатов автоматизированной эндотелиальной кератопластики, выполненной по собственной методике, у больных с буллезной кератопатией.
Материалы и методы исследования
С 2006 по 2008 год нами прооперировано 18 пациентов (18 глаз) в возрасте от 67 до 84 лет. Все пациенты имели псевдофакичную буллезную кератопатию с болевым синдромом. Острота зрения до операции в среднем составляла 0,02 ± 0,01. Сопутствующая глаукома имелась у 11 больных (11 глаз). Из них: у 3 пациентов в анамнезе имелась оперированная компенсированная глаукома 2-3 стадии, у 3 наблюдалась декомпенсация внутриглазного давления на фоне ранее оперированной глаукомы 2-3 стадии, компенсированная глаукома 2-3 стадии на медикаментозном режиме отмечена у 4 пациентов, декомпенсированная у 1. На 4 глазах имелась артифакия с переднекамерной ИОЛ. На 1 глазу наблюдали выпадение части оптического элемента заднекамерной ИОЛ в переднюю камеру, на 1 - дислокацию грибовидной зрачковой ИОЛ.
Операцию выполняли следующим образом: после проведения ретробульбарной анестезии микрокератомом «MORIA One» формировали лоскут на ножке основанием к носу глубиной около 250 µm, 9-9,5 mm в диаметре. После откидывания лоскута трепаном 6,5-7,1 mm иссекали глубокие слои стромы, десцеметову мембрану и эндотелий. Из донорского глаза получали трансплантат аналогичных слоев после срезания микрокетатомом передних слоев роговицы донорского глаза толщиной около 250 µm. Диаметр трансплантата всегда превышал на 0,3-0,5 mm. размер ложа реципиента. Дополнительно, при доступе «открытое небо», производили замену переднекамерной ИОЛ на заднекамерную с шовной фиксацией к склере у 5 пациентов, переднюю витрэктомию у 5, репозицию ИОЛ в 1 случае и пластику радужки в 3. Трансплантат укладывали в ложе реципиента, покрывали лоскутом на ножке передних слоев стромы. Лоскут фиксировали непрерывным швом 10-0. Переднюю камеру восстанавливали воздухом. Трансплантат фиксировали в ложе без швов при помощи воздуха и адгезии срезанных поверхностей у 6 пациентов. В 12 случаях выполняли временную шовную фиксацию транспланта на срок от 3 до 5 дней по нашей методике (патент № 2348388) для предотвращения дислокации трансплантата (рис. 1). Одномоментно с кератопластикой произведена трабекулэктомия с амниотическим вкладышем под склеральный лоскут у 3 пациентов, имплантация силиконового трубчатого дренажа, обернутого консервированной амниотической мембраной в 1 случае [1].
Непрерывный шов, фиксирущий лоскут передних слоев стромы, удаляли через 3-5 месяцев после оперативного вмешательста (рис. 2).
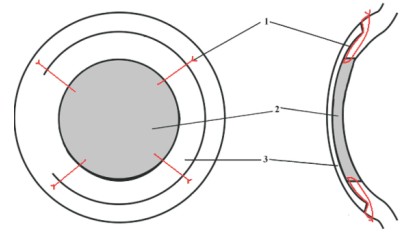
Рис. 1. Схема шовной фиксации трансплантата: 1 - швы; 2 - трансплантат; 3 - лоскут
Результаты исследования и их обсуждение
Трансплантат сохранял прозрачность весь период наблюдения в 67 % случаев (12 глаз). В 22 % случаев (4 глаза) отмечен рецидив кератопатии. В 11 % (2 глаза) на фоне декомпенсации предшествующей кератопластике глаукомы произошел краевой лизис роговичного лоскута с последующим помутнением трансплантата и передних слоев роговицы.
Острота зрения через 1,5 месяца после удаления шва, фиксирующего лоскут передних слоев стромы составила в среднем 0,13 ± 0,08 без коррекции и 0,33 ± 0,14 с максимальной очковой коррекцией. В случаях краевого лизиса лоскута на фоне повышенного внутриглазного давления ухудшение остроты зрения по сравнению с дооперационной не наступило.
Дополнительными причинами, снижающими остроту зрения, были: макулодистрофия - 4 глаза, глаукомная нейропатия - 8 глаз, вторичная катаракта - 3 глаза.
Величина астигматизма по данным рефрактометрии через 1,5 месяца после удаления шва, фиксирующего лоскут передних слоев стромы, варьировалась от 0,37 до 8,0 дптр, составляя в среднем 4,05 ± 2,02 дптр. Сферический компонент был в пределах от 0 до 3,75 дптр, составляя в среднем 1,8 ± 1,14 дптр. Роговичный астигматизм был от 1,47 до 7,0 дптр. со средним значением 3,63 ± 1,71 дптр. Из исследования исключены два глаза с краевым лизисом переднего лоскута роговицы.
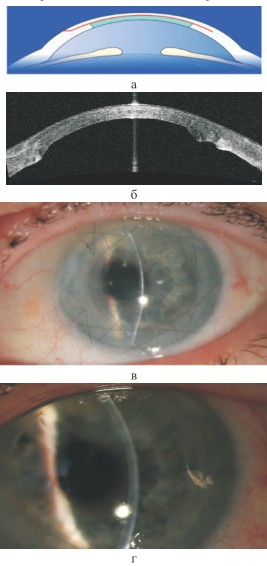
Рис. 2. Передний отрезок глаза после задней послойной кератопластики с формированием поверхностного лоскута роговицы: а - схематическое изображение; б - по данным ОСТ переднего отрезка глаза; в - фото через 1 месяц после операции; г - фото через 7 месяцев после операции
Количество эндотелиальных клеток по данным зеркальной микроскопии к 6 месяцам после операции составляло от 1450 до 2530, в среднем 2026 ± 328 клеток/мм², и постепенно уменьшалось к концу года к количеству от 1360 до 2350, в среднем до 1669 ± 280 клеток/мм². Ко второму году наблюдения среднее значение клеток снизилось до 1413 ± 470, а к третьему году до 1196 ± 462. Данные зеркальной микроскопии подтверждались данными конфокальной прижизненной микроскопии (Confoscan IV NIDEK).
Толщина роговицы через 1 год после операции - от 500 до 565 µm (среднее 521,4 ± 18,9 µm).
При изучении биомеханических свойств роговицы в сроки исследования от 1,5 месяцев до 2,5 лет с помощью пневмотонометрии с динамической двунаправленной апланацией роговицы (Ocular Response Analyzer, Reichert) выявлено умеренное снижение показателей гисторезиса и коэффициента резистентности по сравнению с общепринятой нормой и неоперированным глазом. Определенных тенденций изменения биомеханики в зависимости от сроков наблюдения после операции не отмечено. Гистерезис роговицы составил от 6,1 до 10,3 (среднее 7,8 ± 1,1). Коэффициент резистентности - от 5,1 до 9,7 (среднее 7,7 ± 1,2).
По данным конфокальной прижизненной микроскопии (Confoscan IV NIDEK), к концу первого года наблюдается практически нормальная цитоархитектоника эпителия, стромы, как в области лоскута, так и трансплантата, эндотелия. Место среза микрокератомом определяется по небольшому количеству депозитов и повышенной рефлективности.
У обследуемой группы больных выявлены следующие послеоперационные осложнения:
- дислокация трансплантата без шовной фиксации на следующий день после операции отмечена у 1 пациента, произведена репозиция;
- поскератопластическая глаукома - 4 пациента. Все 4 пациента имели предшествующую кератопластике компенсированную на медикаментозном режиме глаукому, в 3 случаях ранее оперированную. Декомпенсация наступала в сроки от 1 до 3 месяцев после кератопластики, и в 3 случаях потребовалось повторное антиглаукоматозное хирургическое вмешательство;
- 2 случая краевого лизиса лоскута, что мы связываем с подъемом внутриглазного давления в сроки от 1 до 1,5 месяцев после операции;
- рецидив дистрофии роговицы - 4 пациента. Возможными причинами осложнений явились киста радужки с формированием плоскостной передней синехии, повторная дислокация грибовидной ИОЛ, антиглаукоматозная дренажная система.
Заключение
Эндотелиальная автоматизированная кератопластика у больных с буллезной кератопатией позволяет добиться достаточно высокой частоты прозрачного приживления трансплантата при относительно низком риске реакции тканевой несовместимости. Период послеоперационной реабилитации при данном способе проведения операции значительно короче, чем при сквозной кератопластике. В то же время рефракционные нарушения и потери эндотелиальных клеток сопоставимы. В отличие от эндотелиальных кератопластик через тоннельные разрезы, толщина роговицы после операции близка к нормальной, а доступ «открытое небо» является более удобным для сочетанных интраокулярных процедур на переднем отрезке глаза. Предложенный способ временной шовной фиксации трансплантата обеспечивает его надежную адаптацию, предотвращая дислокацию.
Рецензенты:
Хадарцев А.А., д.м.н., профессор, заведующий кафедрой «Внутренние болезни» медицинского института ФГОУ ВПО «Тульский государственный университет», г. Тула;
Киреев С.С., д.м.н., заведующий кафедрой «Анестезиология и реаниматология» медицинского института ФГОУ ВПО «Тульский государственный университет», г. Тула.
Работа поступила в редакцию 29.11.2012.



