В настоящее время отечественные производители выпускают несколько моделей портативных диодных лазерных скальпелей ближнего инфракрасного диапазона (0,78-1,40 мкм), предназначенных для хирургии и эндоскопии, которые сопровождаются сугубо технической документацией без предоставления конкретных методик применения, в частности в хирургической внутрипросветной эндоскопии желудочно-кишечного тракта.
Неоспоримыми преимуществами новых лазерных скальпелей по сравнению с предшествующими моделями различных твёрдотельных лазеров являются малые габариты и масса, встроенное воздушное охлаждение, питание от обычной сети переменного тока, простота в эксплуатации и текущем техническом обслуживании.
Но чтобы успешно применять мощное лазерное излучение в хирургии и эндоскопии с максимальной безопасностью для пациента, необходимо иметь чёткое представление о результатах воздействия данного излучения на биологические ткани. В этом контексте доклинические исследования на суррогате живой ткани [2] или на различных образцах естественных биологических тканей [3] являются фундаментом, на котором базируется разработка оптимальных методик клинического применения высокоэнергетического лазерного излучения.
Хорошо изученным и успешно применяемым на протяжении последних двадцати лет в хирургии и эндоскопии является высокоэнергетический твёрдотельный лазер, излучающий на длине волны 1,064 мкм, где в роли активной среды выступает кристалл алюмоиттриевого граната с вкраплениями неодима (Nd: YAG-лазер 1,064 мкм). Данный вид лазерного излучения также относится к ближнему инфракрасному диапазону спектра оптического излучения. Поэтому знание особенностей его воздействия на биологические ткани целесообразно для предварительной оценки ожидаемого эффекта воздействия на биологические ткани диодного лазерного скальпеля, излучающего на λ = 0,97 мкм.
Полной идентичности воздействия на биологические структуры лазерного излучения 1,064 и 0,97 мкм быть не может из-за имеющейся и весьма существенной разницы поглощения в воде. Лазерное излучение 0,97 мкм лучше поглощается водой, поэтому проникает в ткани на меньшую глубину одновременно с более ранним достижением порога абляции по сравнению с излучением 1,064 мкм. При прохождении через сантиметровый слой воды 60 % излучения 0,97 мкм проходит, а остальные 40 % поглощаются. В идентичных условиях при λ = 1,064 мкм проходит 85 %, а поглощается только 15 % излучения [7]. По мнению Рошаля Л.М. и Брянцева А.В [5], благодаря этой особенности хорошие коагулирующие свойства лазерного излучения с длиной волны 0,97 мкм сочетаются с существенно меньшей по сравнению с Nd: YAG-лазером глубиной термического поражения, что имеет немаловажное клиническое значение.
Norberto L., Polese L. et al. [6] сообщили об опыте применения диодного лазерного скальпеля Dornier Medilas D (λ = 0,94 мкм, максимальная выходная мощность 60 Вт). Данный лазер успешно применялся бесконтактным способом через фиброколоноскоп с целью абляции крупных колоректальных аденом у иноперабельных пациентов. Тем не менее лазерное излучение 0,94 мкм заметно уступает излучению 0,97 мкм по эффективности поглощения в воде и оксигемоглобине.
Глубина проникновения зависит не только от поглощения, но и от рассеяния излучения в биологической ткани. Выраженное влияние на процесс распространения лазерного излучения оказывает изменение свойств биологической ткани под его воздействием, например, обугливание. Поэтому точные значения глубины прогрева биологической ткани могут быть получены только из эксперимента [1].
Цели исследования
Визуальная оценка глубины коагуляционного некроза, возникающего в результате дистанционного и контактного лазирования пластинчатых препаратов печени свиньи при различных значениях выходной мощности и экспозиции непрерывного высокоэнергетического лазерного излучения 0,97 мкм.
Доклиническая экспресс-оценка безопасности применения высокоэнергетического лазерного излучения 0,97 мкм для абляции полипов толстой кишки, отличающейся от других отделов кишечника наименьшей толщиной стенки.
Материалы и методы
Объектом воздействия лазерного излучения были прямоугольные пластинчатые препараты, приготовленные из свежей печени свиньи (не более суток с момента забоя здорового животного). Препараты изготовлялись таким образом, чтобы одна сторона была представлена серозной оболочкой, а другая - срезом паренхимы. Размер стороны прямоугольного препарата не превышал 2,5 см, толщина колебалась от 0,2 до 0,4 см. Поскольку ткань печени, как и ткань кишечника, является водонасыщенной биологической тканью, изготовленные из неё пластинчатые препараты служили моделью кишечной стенки с её прижизненной толщиной. Дополнительным критерием выбора для эксперимента именно ткани печени послужило наличие чёткой, хорошо определяемой невооружённым глазом границы между зоной коагуляционного некроза и визуально неизменённой тканью. Микроскопическая оценка перифокальной девитализации в зоне коагуляционного некроза не проводилась, поскольку эффект тепловой девитализации не имеет решающего значения для оценки риска перфорации полого органа.
Источником лазерного излучения 0,97 мкм служил диодный лазерный скальпель «ЛС-0,97-ИРЭ-Полюс» (Фрязино, Россия, 2002), (рис. 1).

Рис. 1. Диодный лазерный скальпель «ЛС-0,97-ИРЭ-Полюс»
Лазерное излучение при дистанционном лазировании подводилось к препаратам через гибкое, покрытое полиэтиленовой оболочкой кварцевое моноволокно диаметром 600 мкм таким образом, чтобы диаметр светового пятна пилотного лазера составлял 0,5 см. Торец световода был срезан под углом 90° и направлен перпендикулярно к плоскости препарата, чтобы световое пятно пилотного лазера представляло собой правильную окружность с равномерным распределением световой энергии по площади (рис. 2). Фиксация световода в заданном положении проводилась с помощью металлического держателя и лабораторного штатива.
Применялся только непрерывный режим лазерного излучения, имеющий ведущее значение для достижения фотокоагуляции биологических тканей.
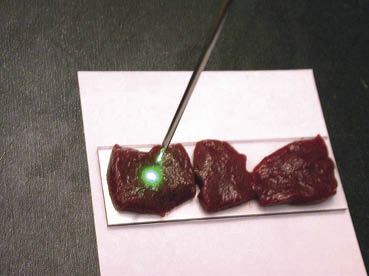
Рис. 2. Вид светового пятна на препарате
Препараты в момент испытания располагались на предметном стекле, расположенном на металлическом поддоне с тефлоновым покрытием.
Заданное значение выходной мощности лазерного излучения на конце световода, высвечиваемое на цифровом табло передней панели лазерного скальпеля, устанавливалось регулятором мощности и контролировалась с помощью встроенного в лазерный скальпель измерителя мощности.
Экспозиция дистанционного облучения препаратов контролировалась с помощью секундомера. Использовались значения выходной мощности 12, 9 и 6 Вт с пошаговой экспозицией от 10 до 1 с. Один препарат облучён в течение 15 с при выходной мощности на конце световода 12 Вт.
Контактное лазирование проводилось методом множественных прерывистых точечных контактов конца световода с поверхностью препарата. Продолжительность точечных контактов и перерывов между ними составила 1-2 с при выходной мощности 12 Вт на конце световода. Точечные контакты наносились до получения равномерного коагуляционного некроза с карбонизацией большей части площади поверхности препарата.
Фотосъёмка хода эксперимента выполнялась цифровой фотокамерой Nikon coolpix 4500.
Результаты исследования и их обсуждение
После проведения бесконтактного лазирования пластинчатого препарата печени со стороны паренхимы в течение 15 с чётко визуализировалась зона коагуляционного некроза. На обратной стороне препарата, покрытого висцеральной брюшиной, также чётко визуализировалась округлая зона некроза серозной оболочки. На поперечном разрезе препарата - явный коагуляционный некроз на всю толщу препарата.
В результате дистанционного лазирования препаратов при выходной мощности 12 Вт с экспозицией от 10 до 1 с визуально определялся коагуляционный некроз на облучённой поверхности во всех случаях, за исключением экспозиции 1 с. При этом чётко отмечалось убывание выраженности и диаметра некроза по мере уменьшения длительности экспозиции. На разрезе отмечался коагуляционный некроз на всю толщину препарата при экспозиции от 10 до 7 с включительно. При экспозиции 6 с отмечался некроз на глубину до 2/3 толщины препарата, при 5-3 с - на глубину до 1/2, а при 2 с - на глубину до 1/3 толщины препарата. При экспозиции 1 с видимый некроз отсутствовал.
Картина коагуляционного некроза при выходной мощности 9 Вт существенно не отличалась от таковой при 12 Вт при значениях экспозиции от 10 до 7 с включительно. Зато при последующем посекундном снижении экспозиции отмечалось явное уменьшение глубины видимой зоны некроза. При экспозиции 6 и 5 с глубина некроза составила не более 1/2 толщины препарата, а при 4 с - не более чем 1/3.
При выходной мощности 6 Вт дистанционное лазирование сопровождалось видимым некрозом лишь при экспозиции от 10 до 8 с включительно. При этом коагуляционный некроз проникал в глубину на 1/2 и 1/3 толщины препарата при экспозиции 10 и 9 с соответственно.
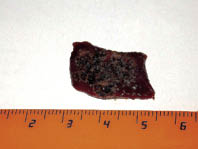
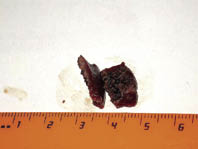
Контактное лазирование при выходной мощности 12 Вт с прерывистой точечной экспозицией 1-2 с не сопровождалось некрозом на всю толщину, а преимущественно на ½ толщины препарата, что имеет важное клиническое значение (рис. 3). Отсутствие тотального некроза обусловлено именно контактным методом вапоризации, когда быстро достигаемое испарение является причиной эффективного охлаждения, которое препятствует глубокому проникновению тепла. Однако существенным фактором здесь является продолжительность точечной экспозиции, так как при значениях последней 3-6 с наблюдался коагуляционный некроз на глубину до 3 мм.
а б
Рис. 3. Контактное лазирование: (а) вид со стороны паренхимы, (б) на поперечном
разрезе. Видимая зона некроза не проникает на всю толщу препарата
Проведённый эксперимент по дистанционному лазированию свидетельствует о том, что высокоэнергетическое лазерное излучение 0,97 мкм обладает значительной проникающей способностью и вызывает коагуляционный некроз на всю толщину пластинчатого препарата печени при среднем значении толщины препарата 0,3 см, относительно длительной экспозиции (7-10 с) и выходной мощности 9-12 Вт. Подобное дистанционное воздействие можно считать фатальным для такого тонкостенного полого органа, каким является толстая кишка. В то же время дистанционное лазирование при тех же выходных параметрах, но при экспозиции не более 5-6 с может найти клиническое применение для абляции колоректальных новообразований плоского типа, выступающих над уровнем слизистой на 3-5 мм.
Ориентируясь на пластинчатый препарат печени как на модель кишечной стенки, наиболее безопасным при дистанционном лазировании предположительно можно считать выходную мощность 6 Вт при экспозиции до 7-9 с и диаметре светового пятна 0,5 см, так как при этих значениях глубина коагуляционного некроза в эксперименте не превышала 0,2-0,3 см.
Контактное лазирование поверхности водонасыщенной ткани, каковой является ткань печени, методом множественных точечных контактов с экспозицией 1-2 с на один контакт относительно безопасно даже при выходной мощности 12 Вт и также может найти применение при лазерной фотодеструкции полипов кишечника плоского типа. В данном случае лазерное излучение более управляемо и менее инвазивно благодаря охлаждению ткани за счёт испарения при быстром достижении порога вапоризации.
Прерывистая вапоризация ткани печени при экспозиции 3-6 с на контакт и выходной мощности 12 Вт сопровождается образованием коагуляционного некроза толщиной до 3 мм. С одной стороны, это обстоятельство можно считать благоприятным для лазерной хирургии печени или селезёнки, поскольку является залогом надёжного гемостаза. С другой стороны, контактная методика при данных значениях экспозиции и выходной мощности имеет обоснованные ограничения при удалении колоректальных полипов, так как зона краевого некроза вследствие вапоризации патологической ткани может проникнуть на всю толщу кишечной стенки и послужить причиной перфорации.
Выводы
Высокоэнергетическое лазерное излучение 0,97 мкм обладает высокой проникающей и коагулирующей способностью в водонасыщенной биологической ткани.
Выраженные проникающие свойства лазерного излучения 0,97 мкм проявляются не только при дистанционном, но и при контактном лазировании с экспозицией более 3 с.
Благодаря хорошим коагулирующим свойствам лазерное излучение 0,97 мкм может с успехом применяться в лазерной хирургии кровенасыщенных органов.
Применение диодного лазерного скальпеля «ЛС-0,97» можно обоснованно рекомендовать для безопасного удаления некрупных полипов плоского типа, локализующихся в прямой кишке ниже уровня тазовой брюшины.
Возможность использования высокоэнергетического лазерного излучения 0,97 мкм с целью фотоабляции полипов, локализующихся в толстой кишке проксимальнее уровня тазовой брюшины, нуждается в дальнейшем изучении, прежде всего с точки зрения безопасности для пациента.
Список литературы
- Гаращенко Т.И., Богомильский М.Р., Минаев В.П. Лечение ЛОР-заболеваний с использованием лазерных скальпелей. - Тверь: ООО «Губернская медицина», 2001. - 52 с.
- Суррогат живой ткани для тестирования хирургических лазеров / А.И. Неворотин, А.А. Жлоба, И.К. Ильясов [и др.] // Бюлл. эксп. биол. мед. - 1996. - №11. - С. 597-600.
- Анализ лазерных поражений живой ткани / А.И. Неворотин, А.А. Воднев, Д.П. Агапов [и др.] // Актуальные проблемы лазерной медицины: сборник научных трудов (ред. Н.Н. Петрищев). - СПб.: Изд-во СПб ГМУ, 2001. - С. 46-63.
- Прикладная и лазерная медицина: учебное и справочное пособие / под. ред. Х. -П. Берлиена, Г.Й. Мюллера; пер. с нем. - М.: АО «Интерэксперт», 1997. - 356 с.
- Рошаль Л.М., Брянцев А.В., Минаев В.П. Применение полупроводникового лазерного скальпеля в лапароскопической хирургии детского возраста: методические рекомендации. - Департамент здравоохранения Правительства Москвы, 2008. - 34 с.
- Norberto L., Polese L. et al. Laser photoablation of colorectal adenomas. A 12-year experience // Surg Endosc. - 2005. - №19. - Р. 1045-1048.
- Palmer K.F., Williams D. Optical properties of water in the near infrared // J. Opt. Soc. Am., 64, 11-7-1110, (1974).
Рецензент -
Колесов Владимир Николаевич, д.м.н., профессор кафедры нейрохирургии Саратовского государственного медицинского университета.



